МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИИ
Ось X — этапы исследования:
1 — до переливания;
2 — 30 минут после переливания;
3 — 4 часа после переливания.
График 2. Изменение лабораторных показателей в зависимости от переливания Инфукола 6% — 200/0,5.
Центр сердечно-сосудистой хирургии «Лосиный остров» МПС России
Материалы международной научно-практической конференции
БЕСКРОВНАЯ ХИРУРГИЯ НА ПОРОГЕ XXI ВЕКА
(17–18 марта 1999 г.)
(17–18 марта 1999 г.)
Под редакцией зав. кафедрой госпитальной хирургии РУДН профессора Ю. В. Таричко
ISBN 5-7873-0006-9
Содержание
1. ПРЕДИСЛОВИЕ
2. НИ МИНУТЫ БОЛИ, НИ ЛИШНЕЙ КАПЛИ КРОВИ У ПАЦИЕНТА
3. СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ОСТРОЙ КРОВОПОТЕРИ[1]
4. КРОВОПОТЕРЯ И РЕГУЛЯЦИЯ КРОВООБРАЩЕНИЯ В ХИРУРГИИ
5. ПРИМЕНЕНИЕ ИНФУКОЛА ДЛЯ КОРРЕКЦИИ ГИПОВОЛЕМИИ В ИНТРАОПЕРАЦИОННОМ ПЕРИОДЕ
6. ОПЫТ АУТОДОНОРСТВА И СБЕРЕЖЕНИЯ КРОВИ В СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ
7. ОПЫТ ПРОВЕДЕНИЯ БЕСКРОВНЫХ ОПЕРАЦИЙ НА ОТКРЫТОМ СЕРДЦЕ
8. ОСОБЕННОСТИ ИНТРАОПЕРАЦИОННОГО ОБЕСПЕЧЕНИЯ БЕСКРОВНОЙ ХИРУРГИИ У БОЛЬНЫХ ИБС
9. ПУТИ СОХРАНЕНИЯ КРОВИ ПАЦИЕНТА ПРИ ОПЕРАЦИЯХ НА ОТКРЫТОМ СЕРДЦЕ
10. РЕИНФУЗИЯ КАК ИНТРАОПЕРАЦИОННЫЙ МЕТОД СБЕРЕЖЕНИЯ КРОВИ ПАЦИЕНТОВ В СЕРДЕЧНОСОСУДИСТОЙ ХИРУРГИИ
11. ПРИНЦИПЫ ЗАМЕСТИТЕЛЬНОЙ ТЕРАПИИ ТРОМБОЦИТОПЕНИЧЕСКОГО СИНДРОМА ПРИ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ У ГЕМАТОЛОГИЧЕСКИХ БОЛЬНЫХ
12. ИНТРАОПЕРАЦИОННЫЙ АУТОЗАБОР КРОВИ КАК СПОСОБ ЕЁ СОХРАНЕНИЯ ПРИ ОПЕРАЦИЯХ У ОРТОПЕДИЧЕСКИХ БОЛЬНЫХ
13. ПРИМЕНЕНИЕ АУТОТРАНСФУЗИЙ В УСЛОВИЯХ МНОГОПРОФИЛЬНОЙ БОЛЬНИЦЫ
14. ПРИМЕНЕНИЕ АУТОГЕМОТРАНСФУЗИИ В УСЛОВИЯХ МНОГОПРОФИЛЬНОЙ БОЛЬНИЦЫ
15. ЭФФЕКТИВНОСТЬ ВОСПОЛНЕНИЯ КРОВОПОТЕРИ АУТОКРОВЬЮ ПРИ ВНЕМАТОЧНОЙ БЕРЕМЕННОСТИ
16. ВЛИЯНИЕ ПЕРЕЛИВАНИЯ КОМПОНЕНТОВ КРОВИ НА ВЕРОЯТНОСТЬ ПОВТОРНОГО КРОВОТЕЧЕНИЯ У БОЛЬНЫХ С ГАСТРОДУОДЕНАЛЬНЫМИ ЯЗВАМИ
17. ОЦЕНКА ЭФФЕКТИВНОСТИ ПЛАЗМОЗАМЕЩАЮЩЕГО ПРЕПАРАТА ГЕЛОФУЗИН В ИНТЕНСИВНОЙ ТЕРАПИИ ХИРУРГИЧЕСКИХ БОЛЬНЫХ
18. КРОВЕСБЕРЕГАЮЩИЕ ПРИЁМЫ ПРИ СПЛЕНЭКТОМИИ У ГЕМАТОЛОГИЧЕСКИХ БОЛЬНЫХ
19. МЕТОДЫ СБЕРЕЖЕНИЯ КРОВИ В АКУШЕРСКО-ГИНЕКОЛОГИЧЕСКОЙ КЛИНИКЕ
20. ЦЕНТРЫ БЕСКРОВНОЙ МЕДИЦИНЫ — ПОЧЕМУ ВРАЧИ НАЧАЛИ ОБХОДИТЬСЯ БЕЗ ДОНОРСКОЙ КРОВИ
21. УСПЕШНЫЕ ОПЕРАЦИИ НА СЕРДЦЕ БЕЗ ПЕРЕЛИВАНИЯ КРОВИ
22. ТОЛЕРАНТНОСТЬ К АНЕМИИ. СТРАТЕГИЯ БЕСКРОВНОЙ ХИРУРГИИ — РОЛЬ АНЕСТЕЗИОЛОГА
1. ПРЕДИСЛОВИЕ
Наше поколение воспитано на незыблемом убеждении о бесспорной пользе донорской крови для больных с самыми различными заболеваниями. В основе такого убеждения лежит многолетняя практика врачей, рассматривающих донорскую кровь как лекарство от всех болезней. И действительно, часто переливание крови оказывало разительный лечебный эффект. Так с годами у медицинской общественности сложилась своеобразная идеология, поощряющая переливания крови даже там, где можно было вполне обойтись и без этого, и блокирующая современные бескровные методы лечения.
Но сейчас, на пороге XXI века, многие врачи сходятся во мнении, что польза от переливания крови год от года уменьшается, а на первый план выступают отрицательные моменты этой процедуры, и в первую очередь подчёркивается опасность её проведения для больного.
Среди проблем, связанных с переливанием крови, выделяют реальную возможность заражения пациента различными инфекциями, получения тяжёлых трансфузионных реакций, неудовлетворённую потребность здравоохранения в донорской крови и т.д.
Наша конференция целиком посвящается проблемам бескровной хирургии. Она стоит в числе первых у нас в стране и призвана обсудить перспективы развития отрасли здравоохранения, которую называют «медициной будущего».
Поводом для проведения конференции стали значительные успехи российских исследовательских технологий бескровной медицины и необходимость скорейшего внедрения их в жизнь.
Что же такое бескровная хирургия? За этим понятием стоит комплекс фармацевтических, терапевтических и хирургических методов, предотвращающих потерю крови при операциях и помогающих организму больного функционировать с пониженным уровнем объёма крови или её компонентов.
Основные методы бескровной хирургии достаточно просты и, при желании, доступны. Вот некоторые из них: сведение к минимуму кровопотери во время операции за счёт использования электрокоагуляции или лазерных скальпелей; обработка раны различными «клеями», способствующими свёртыванию крови; использование кровезаменителей; восстановление потерянной крови за счёт использования оборудования для сбора крови с операционного поля (Cell Saver); комплекс мероприятий, позволяющий наиболее рационально использовать кровь пациента, и т.п.
Наиболее сложным в этой проблеме представляется внедрение в сознание врачей новой идеологии и убеждение их в её прогрессивности.
В конференции участвуют видные специалисты по бескровной медицине из США, но отличительной её особенностью является большое количество докладов отечественных специалистов, имеющих положительный практический опыт по внедрению в жизнь принципов бескровной хирургии, исходя в первую очередь из интересов больного, заботы о его благе.
Думаю, что недалёк тот день, когда предлагаемые методики станут доступными широкой медицинской практике и пациенты в наших клиниках предпочтут для себя бескровную хирургию.
Профессор Ю. В. Таричко, заведующий кафедрой госпитальной хирургии Российского университета дружбы народов, руководитель Центра бескровной сердечно-сосудистой хирургии МПС.
2. НИ МИНУТЫ БОЛИ, НИ ЛИШНЕЙ КАПЛИ КРОВИ У ПАЦИЕНТА
Академик РАМН Б. В. Петровский.
Научный центр хирургии РАМН, Москва, Россия.
Научный центр хирургии РАМН, Москва, Россия.
Прогресс хирургии в XX веке во многом связан с достижениями анестезиологии, реаниматологии и трансфузиологии, в частности с внедрением в практику методов переливания крови.
Тысячи людей в мирное время и на войне своим спасением обязаны переливанию донорской крови. До последнего времени переливание крови считалось неотъемлемой частью каждой операции.
Необходимость переливания крови вызвала широкое развитие такого социально-медицинского явления, как донорство. Армия доноров даже в небольших странах насчитывает миллионы человек. Количество единиц крови, переливаемой ежегодно больным, также исчисляется миллионами доз. Кровь стали называть даром жизни, а её переливание считают практически безопасным.
К сожалению, в наше время среди доноров регистрируется всё больше социально неустроенных людей. Громадный клинический опыт позволил выявить и отрицательные стороны переливания крови, связанные с риском развития тяжёлых, порой смертельных осложнений. Прежде всего это гемолитические реакции и передача возбудителей различных инфекций. Так, по статистике примерно 1 из 100 переливаний сопровождается лихорадкой, ознобом или крапивницей. 1 из 6000 переливаний эритроцитов приводит к развитию тяжёлой гемолитической трансфузионной реакции, которая может проявиться сразу или через несколько дней после трансфузии, привести к тяжёлой почечной недостаточности, шоку, внутрисосудистому свёртыванию крови и даже — к смерти.
В настоящее время публикуются данные об отрицательном влиянии донорской крови на иммунную систему больного. Некоторые исследования показывают, что больные, получившие кровь, более предрасположены к инфекции.
Имеются сообщения о неблагоприятном воздействии трансфузии крови на результаты хирургического лечения злокачественных новообразований и большей вероятности рецидива опухоли, что связывают также с возможным угнетением иммунной системы.
Острое беспокойство врачей вызывает также возможность переноса с донорской кровью возбудителей различных заболеваний. Подобных заболеваний очень много, и, в первую очередь, к ним относятся такие инфекционные болезни, как сифилис, цитомегаловирус, малярия. Имеются данные о передаче с кровью вируса герпеса, инфекционного мононуклеоза, токсоплазмоза. Список таких заболеваний растёт, и среди них могут быть неизвестные врачам данной местности болезни, что связано с большой миграцией населения.
Две другие инфекции не просто пугают, а внушают ужас и врачам, и пациентам.
Около 5% реципиентов в США заболевают впоследствии гепатитом. Это примерно 175 000 человек в год. Около половины из них становятся хроническими носителями, примерно у 1 из 5 развивается цирроз или рак печени. 4000 человек в год умирают. В печати сообщают о всё новых вирусах гепатита и о ненадёжности тестов на обнаружение их в крови.
С 1981 г. мы знаем о чуме XX века — СПИДе. Вскоре после его появления было выяснено, что СПИД вызывается вирусом иммунодефицита человека (ВИЧ), который может переноситься кровью и её продуктами. Опасность заключается в том, что современные тесты на СПИД ненадёжны, люди могут годами носить вирус СПИДа без обнаружения его современными косвенными способами, сдавать кровь с отрицательным результатом при тестировании и заражать таким образом других. Опасность передачи СПИДа через кровь и её компоненты на сегодняшний день не может быть полностью устранена.
Понятна поэтому наблюдаемая в последние годы в мире тенденция к сокращению переливания донорской крови.
В этой связи сегодня особенно важным является ответ на вопрос: можно ли на практике ограничить или отменить использование чужеродной донорской крови, не подвергая при этом жизнь и здоровье хирургических больных неоправданному риску.
Научные аспекты этого вопроса предстоит обсудить на настоящей конференции.
В практическом отношении наиболее важными представляются сообщения о толерантности больных к анемии и её допустимом пределе, способах восполнения кровопотери бескровными методами и основных клинических принципах сбережения крови пациентов.
Мы знаем, что у больных с резкой и значительной потерей крови развивается шоковое состояние. При этом возникает необходимость остановки кровотечения и восстановления объёма циркулирующей крови. Для восстановления объёма циркулирующей крови предложено много эффективных кровезаменителей. Самый старинный из них — физиологический раствор, который сослужил хорошую службу хирургам во многих ситуациях. Теперь используют декстран, желатиновый раствор, раствор Рингера с лактатом, гидроксиэтилкрахмал и другие, восполняя этими веществами объём потерянной крови.
Для восполнения кислородопереносящей функции крови используются искусственные переносчики кислорода, такие, как перфторан, часто применяется гипербарическая оксигенация (ГБО). Однако и здесь имеются препятствия — фтор остаётся в организме, ГБО сопровождается риском.
Новые железосодержащие препараты помогают быстро восстанавливать гемоглобин больного.
Большое значение имеет разработка различных методов сбережения крови в хирургии. Это направление следует рассматривать как новую медицинскую идеологию, основной формой которой является внедрение бескровной хирургии. В идеале необходимо вообще исключить применение донорской крови на операциях без острой необходимости, оставляя её запасы, чаще всего ограниченные, для действительно критических ситуаций.
Свой вклад в развитие этой проблемы внесут все участники хирургического процесса и, прежде всего, хирурги и анестезиологи.
Содержанием этой работы является внедрение в практику новых устройств, уменьшающих кровотечение при рассечении тканей; внедрение новых хирургических методик, позволяющих выполнять вмешательства без больших доступов (рентгенохирургия, эндоскопическая хирургия); использование различных вариантов аутодонорства; при неизбежной кровопотере — применение различных механических методов и устройств для сохранения крови и реинфузии её пациенту.
Важно отметить, что во всех случаях значительной периоперационной кровопотери, никакой отдельно взятый метод не бывает достаточен, чтобы полностью уйти от переливания крови. Для обеспечения этого замысла требуются хорошее специальное оборудование и подготовленные специалисты, работающие по специально принятым в клинической практике программам бескровной хирургии.
В мировой практике накоплен немалый опыт бескровных операций (в том числе у пациентов, отказывающихся от переливания крови по религиозным соображениям), о чём свидетельствуют, в частности, сообщения крупных хирургических авторитетов (М. Дебейки, Д. Кули и др.).
Не менее актуальна в наше время стрессов и психологических катастроф, малых войн и страха перед преступниками борьба с болью в медицинских учреждениях. Многие люди боятся боли при лечении зубов, при ранениях, ожогах, ортопедических манипуляциях и т.д.
Мы помним войну, когда при отступлении наших войск ранения протекали тяжелее, чем при наступлении и после победы. Летальность после операции также соответствовала этой закономерности. Нам нужно более уверенно решать эту проблему в медицине, особенно в хирургии, акушерстве-гинекологии, травматологии и оториноларингологии, офтальмологии, при перевозке больных в машинах скорой помощи и других случаях.
Итак, ни минуты боли, ни капли необоснованной потери крови в медицинских учреждениях.
3. СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ОСТРОЙ КРОВОПОТЕРИ[1]
Академик РАМН А. И. Воробьёв.
Гематологический научный центр РАМН, Москва, Россия.
Гематологический научный центр РАМН, Москва, Россия.
Дорогие друзья! В мире есть много парадоксов — наш институт, теперь уже ставший Гематологическим центром (а в прошлом — первый в мире Институт переливания крови) был создан Александром Александровичем Богдановым. Он был старым революционером и большевиком, одним из создателей (вместе с Лениным) социал-демократической рабочей партии. Он был автором первого учебника политэкономии, в 1908 г. он написал роман «Красная Звезда», в котором рассказывалось, как на корабле с ядерным двигателем один русский социал-демократ летит на Марс. Мы это читали как «Аэлиту» А. Н. Толстого. Толстой художественно обработал роман А. А. Богданова. В романе рассказывалось, что с целью омоложения пожилым переливали кровь молодых. Идея создания Института переливания крови не заключалась в изучении методов восполнения кровопотерь при ранении, она состояла в том, чтобы научиться воздействовать на жизненные силы организма — сделать его здоровее, моложе. Идея сегодня кажется немного странной, однако надо помнить, что институт создали в 1922 г., когда люди не выглядели так, как сегодня — они были худые и бледные, поскольку питались плохо, из-за недостатка мяса у них была анемия. Тогда казалось, что с помощью переливания крови можно всё, в том числе и поднять здоровье. Но прошли десятилетия, сам профессор Богданов погиб от переливания крови (по-видимому, от несовместимости по резус-фактору), причиной смерти была острая почечная недостаточность. За прошедшие годы мы накопили огромный опыт — на сегодняшний день полностью отпали любые назначения переливания с целью какой-либо стимуляции.
Ушли в прошлое разговоры о трофической и гемостатической роли переливания крови. Напротив, нет ничего хуже, когда при ранениях переливают кровь. Сегодня донорскую кровь используют только с заместительной функцией. Однако даже в этой ситуации мы вынуждены были признать, что настоящую кровь перелить нельзя. Крови, как таковой, не существует в бутылке. Безусловно, это звучит парадоксально, но древние говорили, что нельзя дважды войти в одну и ту же реку, поскольку она изменилась. Кровь тоже изменяется — даже при аутотрансфузии (реинфузии своей же крови) вы переливаете не ту самую кровь. Если насасывать шприцем и тут же переливать, можно спровоцировать катастрофу, которая закончится трагически. Кровь надо отмыть, освободив от всего того, что было кровью (кроме эритроцитов) — вот это будет реинфузия. Предоперационной заготовкой цельной крови больного мы не пользовались — заготавливали компоненты крови, помня о том, из чего состоит консервированная кровь. Она содержит эритроциты и плазму, но тромбоциты разрушились и остались в ней, лейкоциты также разрушились и остались, эритроциты образовали конгломераты. Какая же это аутокровь? Это субстанция с выраженными агрессивными свойствами — совсем не то, что у нас в сосудах. Итак, лечение острой кровопотери нельзя оценивать схематично, на примере сообщающихся сосудов, когда некий объём крови выливается, а затем возвращается. Мы это усвоили на тяжких примерах — прежде всего при борьбе с акушерскими кровопотерями.
В нашем Центре есть специальная бригада неотложной гематологической помощи. Она создавалась для терапии сепсиса, шока, тяжёлых гемофилических состояний. Однако как показывает практика, эта помощь используется практически исключительно при острых акушерских кровотечениях. Ещё год назад принимать дежурство на утренней пятиминутке было мучительно стыдно — начинается доклад бригады неотложной помощи: вызов в родильный дом, роды или кесарево сечение и неуправляемое кровотечение … Каждый раз я мог сам продолжить рассказ (о событиях до приезда нашей бригады): … перелили ведро крови (собрав её предварительно у окрестных солдат), потом ампутировали матку, затем была релапаротомия, перевязали подвздошную артерию (вместе с мочеточником) и, наконец, больную доставили к нам или потеряли. Это было системой. Но вдруг наступило время — ни одного вызова. Это было результатом очень неприятных разговоров. Мы говорили врачам: «Вы убийцы! Вы переливаете кровь — вы убийцы». Неверно, что акушерские кровотечения принципиально отличаются от других. Разве женщина не человек? Разве у неё иначе течёт кровь? С той же ситуацией сталкивались урологи лет 20–30 назад, когда не могли остановить кровотечение после травматичной резекции предстательной железы. Только одна медицинская специальность — акушерство — исповедовала совершенно каннибалистскую идею — «капля за каплю», т.е. если женщина потеряла литр крови, надо ей литр вернуть. Я уже говорил, что вернуть ту же кровь мы не можем. У нас нет крови — то, что вы называете кровью, таковой не является. Многим это пришлось усвоить ценой длинных разговоров (грубых и вежливых) и публикаций («Медицинская газета», журнал «Врач», конференции и т.д.). Можно поднять один вопрос, который я долго не задавал сам себе: «Видел ли кто-нибудь смерть от потери кислородоносителя, то есть от нехватки в организме гемоглобина?» (Мне недавно напомнили, что я видел — при пернициозно-анемической коме, а вот от кровотечения?) Нет, не видел. В среднем нашу дежурную бригаду вызывают в роддома слишком поздно — через 12 часов после начала кровотечения. Тем не менее, смертность составляет 4–13% (в отсутствие наших специалистов — 22–47%). Бригада не переливает эритроциты, но переливает много плазмы.
Были проведены эксперименты. У кроликов выливали всю кровь и заменяли раствором, который делает жидкости более текучими. Ни один из кроликов не погиб, хотя они и не очень стойкие животные. Дело в том, что запасы кислородоносителей в организме столь велики, что их убрать в реальных условиях практически невозможно.
Острая кровопотеря — это состояние, над которым эволюция работала гораздо дольше, чем над туберкулёзом, тифом, малярией и т.д. Живое всегда теряло кровь. Клинические признаки: бледность конъюнктив, симптом пустых сосудов, одышка при минимальной физической нагрузке (настоящая одышка — это не учащённое дыхание, это участие лестничных мышц и раздувание ноздрей при акте вздоха), тахикардия — необязательный признак, снижение АД. Мы говорим о массивной кровопотере — это около 30% объёма крови. Старые акушеры знают, что женщина может погибнуть от литрового, даже полулитрового стремительного кровотечения. При этом она гибнет от кровотечения, но не от потери кислородоносителя. Включается физиологическая самозащита, активация тромбоцитов, образование первичного тромба, снижение АД. Всё это направлено на остановку кровотечения.
Врачи нередко забывают о внутренней аутотрансфузии. Зачем человеку нужен такой объём крови (в среднем 7 литров)? Чтобы он мог внезапно побежать, мог ходить по лестнице, энергично напрягать голосовые связки и жестикулировать. Если же лишить человека всего этого, ему нужно гораздо меньше крови. Мускулатура работающая и неработающая содержит кровь 1:20 — при исчезновении нагрузки моментально запустевают капилляры мышц. Обратите внимание, ведь более всего вегетативной симпатической иннервацией снабжены коронарные артерии и аорта. Любой мотив, побуждающий к движению, немедленно обеспечивает усиление снабжения коронарных сосудов, чтобы вызвать тахикардию. В организме всё построено на мышечном обеспечении: головной мозг берёт мало крови, главное — мышцы. Итак, первое, что надо сделать при ранении, родах и т.д. — обездвижить больного (мы сейчас не разбираем ситуацию, когда человек, например, сражается с волком). Сбила машина — лежит, роды — лежит, огнестрельное ранение — лежит. При этом мышцы не работают, происходит внутренняя аутотрансфузия. Снижение температуры связано с падением основного обмена. Падает потребление крови — организм очень серьёзно думает над тем, как компенсировать кровопотерю. Останавливается секреция — почти остановилось мочеотделение, сухость во рту. Происходит централизация кровообращения — организм моментально замыкает его на жизненно важных органах — пустые вены, белая кожа. Отмечаются лёгкий сопор, односложные ответы на вопросы. В такой ситуации мы говорим: «Кровопотеря два литра, надо срочно лить». Лить надо, но не кровь.
Вам несколько парадоксально слышать такое от человека, который должен защищать переливание крови. Однако я не предлагаю всё отменить и полагаться на Господа Бога. Должен быть научно обоснованный подход. Итак, если из 7 литров крови вылилось 3 литра, то это не значит, что осталось 4. Математически это 4, а физиологически — совсем не так. Это было убедительно доказано. Когда мы собрались в космос и стали проводить эксперименты по гиподинамии, выяснилось, что это состояние немедленно (в течение дней, недель) сказывается на остановке эритропоэза. Иначе быть не может, ведь спячка придумана не человеком, а другими млекопитающими — грызунами и всеядными. Если медведь ляжет спать на всю зиму и не остановит эритропоэз, он просто затромбируется. Итак, когда стало ясно, что 7 литров крови нужны для мышечной работы, а не для сна, мы начали понимать, почему при инфаркте возникает анемия (в старые времена, когда мы месяц, держали больного на спине при трансмуральном инфаркте). Ещё один пример: американцы показали, что если раненым до остановки кровотечения переливается кровь и другие жидкости, то в сравнении с той группой, где ничего не переливают, смертность выше (не катастрофически выше, но достоверно). Это было просчитано — больше погибают там, где переливают. Таким образом, если вы не можете перевязать сосуд, то внутривенные инфузии опасны — опасны тем, что вы повышаете АД и срываете тромбообразование.
Я должен вспомнить один эпизод из нашей с вами биографии. Было время, когда переливали трупную кровь. Это предложили наши замечательные хирурги — Шамов, Юдин. Я ещё застал время, когда в институте Склифосовского переливали трупную кровь. При этом исходили из времён Богданова, что вылитая кровь — это та же кровь. Как теперь выяснилось, это ошибка. Вначале кровь в трупе свёртывается. Но затем фибрин, выпадающий в сосудах, ферментативно разлагается на фибрин-мономеры, обладающие фибринолитическим действием. Происходит фибринолиз, растворяются все тромбы в организме. Это позволяло заготовлять трупную фибринолизную кровь. Переливать такую кровь не следует, а для других целей она может куда-то и годится. Но по международным законам трупная кровь, кровь больных — только на выброс. Ещё один пример — стремительные роды. Что такое стремительные роды? Это когда из брюшной полости быстро удаляется около 5 кг объёма. Известно, что и при хорошем поносе у человека голова кружится. Ведь испражнение — это определённая гемодинамическая нагрузка, в брюшную полость проваливается венозная кровь, возникает гипоксия мозга. Женщина, стремительно родившая, даёт коллапс от потери объёма — от провала крови в брюшную полость. Вот другие неблагоприятные факторы (у нас же разное отношение к родам). Одним пришла мысль, что мы произошли от тюленей и поэтому надо рожать под водой. Другим — что надо так обезболить женщину, чтобы ничего не чувствовала. Я вообще-то работал в родильном отделении, хотя сам не рожал (единственное, чего не испытал). Но обезболивая надо помнить, что это не простой процесс. Ещё одна гениальная идея — сменить время родов. Это было у меня на глазах — женщин всячески стимулировали на дневные роды. Почему-то во всём животном мире роды идут ночью — собаки, коровы, лоси. Это отрабатывалось веками, тысячелетиями. Некоторые рекомендовали ускорять роды при помощи массажа матки. У матки двоякая миссия: помимо того, что надо выносить плод, его надо вытолкнуть. Говоря с коагулологических позиций, нужно, чтобы в течение 9 месяцев не было тромбирования плаценты. Это обеспечивается антикоагуляцией. Затем, когда роды произошли и плацента вытолкнута, освобождается кровоточащая площадь с размером с ладонь — это открытая гигантская рана, которую матка должна немедленно закрыть путём сжатия и тромбирования. Таким образом, тканевой тромбопластин, содержащийся в миометрии, поможет затромбировать плодное место. Но если до родов мять матку или при кесаревом сечении рвать её, то тканевой тромбопластин выталкивается в кровяное русло. Это уследить невозможно. Итак, стремительные роды. Вышел плод, вышла плацента. Женщина бледна, плохо отвечает на вопросы. Что же произошло? У неё упало АД из-за провала крови в брюшную полость, что естественно. Однако в крови много тканевого тромбопластина, и этот фактор свёртывания, на фоне снизившегося или остановившегося кровотока, свёртывает всю кровь на периферии — разыгрывается диссеминированное внутрисосудистое свёртывание. Это обычный ферментативный процесс, происходит то же, что у трупов (см. выше). И вдруг женщина, за которой плохо следили, начинает ещё больше бледнеть — врач видит, что из влагалища течёт струйка крови, не свёртываясь на простыне. В чём тут опасность? Как только разыгрался ДВС-синдром, врач решает: «Она теряет кровь, надо ей вернуть кровь».
Диссеминированное внутрисосудистое свёртывание крови проходит две фазы. Первая фаза — гиперкоагуляционная (в акушерстве это бывает очень быстро и обычно пропускается). Гиперкоагуляционная фаза имеет более точную характеристику — полиорганная патология. Прежде всего это мозговая патология: женщина замолкает, не реагирует, когда ей показывают ребёнка, ожидая от неё болезненной, радостной улыбки. Она не реагирует, потому что микросвёртывание в сосудах головного мозга вызывает заторможенность. Из этой фазы легко выйти, быстро перелив свежезамороженную плазму. Затем наступает гипокоагуляционная фаза, когда свёртки крови начинают распадаться, выбрасывая в кровоток продукты деградации фибрина, обладающие фибринолитическим действием. В этот момент у женщины начинается кровотечение. Врачи нередко удаляют матку, что помогает не всегда. В половине случаев идут на релапаротомию, поскольку невозможно перевязать все сосуды, капилляры — идёт паренхиматозное кровотечение. Диагноз этого состояния врач обязан ставить без всяких анализов, это очевидная вещь.
Теперь к вопросу о переливании крови таким больным. Известно, что толщина стенки альвеолы примерно равна диаметру эритроцита, а просвет капилляра составляет 3–4 мкм, там эритроцит сворачивается. Это происходит, чтобы увеличить площадь соприкосновения с альвеолярным воздухом. При ДВС-синдроме лёгкие «заболочены» кровью, эритроциты в сосудах остановились, слиплись. И в это лёгкое, в эту сосудистую сеть переливать кровь? Что же будет? Будет ещё хуже.
Какой уровень гемоглобина надо принимать в качестве критерия для переливания крови при острой кровопотере? Вопрос безграмотен от начала до конца! Вспоминается случай из моей практики. В приёмный покой городской больницы поступает молодая женщина. Диагноз — внематочная беременность. После осмотра я обращаюсь к своему старшему товарищу (замечательному врачу Плотникову Николаю Михайловичу) и говорю: «Белая как полотно, а гемоглобин нормальный». В ответ он захохотал. Действительно, гемоглобин — это количество кислородоносителя в единице объёма. А бледность — это количество единиц объёма. При острой кровопотере уровень гемоглобина никогда не снижается. Он падает, когда нальют больного водой и разбавят кровь. Подумайте о концентрации соли в щах — одна ложка щей или целая кастрюля — концентрация остаётся та же. При этом, конечно, соли меньше в ложке, чем в кастрюле. Но нельзя же путать кубы и километры! Таким образом, уровень гемоглобина — не показатель, речь идёт об острой кровопотере. Я очень прошу не обобщать мои высказывания так: «Воробьёв сказал, что гемоглобин — не показатель». Гемоглобин — нужный показатель, но в другой ситуации. Итак, возвращаясь к предыдущему случаю: что переливание эритроцитов на фоне ДВС-синдрома приводит к остановке оксигенации имеющейся крови и женщина может умереть.
Причины ДВС-синдрома в акушерстве: отслойка плаценты, септический аборт, внутриутробная гибель плода, внематочная беременность, тяжёлый гестоз, кесарево сечение, несовместимость по ABO и по резус-фактору матери и плода. Переливание цельной (и особенно тёплой) крови — это ужасно. Нет ничего глупее термина «переливание тёплой крови». Я сам раньше делал это, но не стесняюсь говорить о своих ошибках. Всего лишь кажется, что это кровь, на самом деле — это сгустки, несмотря на антикоагулянты.
Клиника гипокоагуляционного ДВС-синдрома настолько яркая, что нет необходимости ждать лабораторного подтверждения, теряя драгоценное время. Самый яркий симптом — полиорганная недостаточность. Как её диагностировать? Имеет место лёгкий сопор, быстрая истощаемость. На первый вопрос ответ есть (одно слово), на второй — есть, на третий — с задержкой либо вообще пропускается. Если повторить — она ответит.
— Голова болит?
— Нет (она не скажет: «Голова совершенно не болит»).
— Пить хочется?
— Да.
— Сухость есть во рту?
Всё, больше не отвечает. Энцефалопатия поставлена. Разве требуется подтверждать это какими-то анализами? Далее выслушиваем сердце. Короткая систола или, ещё хуже, эмбриокардия (сердце стучит без разницы систоло-диастолических интервалов). На электрокардиограмме иногда сползают Т-зубцы. «Заболоченность» в лёгких, о которой я говорил, на снимке видна как облаковидные тени. Аускультативно (надо слушать ухом) выявляются очаги бронхиального дыхания, иногда с крепитацией, иногда — без. Появление бронхиального дыхания — признак уплотнения лёгочной ткани, интерстициального отёка. Не следует забывать об уровне трансаминаз в сыворотке. На второй или третий день он повышается, иногда возрастает билирубин. Всё это связано с изменением паренхимы печени в результате микротромбирования. Патология почек — отсутствие мочи или резкая олигурия (150–200 см3 мочи в сутки). Я назвал все органы, доступные прямому анализу. Бывает поражение и других органов, но этих — наиболее отчётливо. Это и есть полиорганная патология.
Тактика лечения: остановка кровотечения, кислород, поддержание АД (кстати, довольно принципиальный и сложный вопрос). Насколько поднимать АД? Ровно настолько, чтобы больной дышал и не более. Поднимая АД слишком высоко, мы срываем тромбы. Оно должно быть минимальным, ориентировочно 60–80/40 мм рт.ст. Мы, конечно, предпочитаем нормальное АД, но ситуация складывается в контексте острой кровопотери. Речь идёт о минутах, десятках минут. Если в эти сроки глупостей не сделать, всё будет хорошо. От анемии на следующий день никто не умирает, всё восстанавливается.
Инфузионные средства: солевые растворы, гидроксиэтилкрахмал, альбумин (для восполнения объёма), свежезамороженная плазма, а уже потом — если будет необходимость — эритроциты. Соотношение плазмы к эритроцитам должно составлять 4–5 к 1. При этом важно помнить, что по статистике в США 1% донорской крови заражён вирусом гепатита C. Вирусом СПИДа — меньше (у нас этот показатель ещё ниже). Однако у них среди белого населения имеется примерно 0,2% носителей гепатита, у нас — 2% носителей по каждому гепатиту, а среди доноров — 6%. Так что переливание, мягко выражаясь, рискованная процедура. Свежезамороженная плазма — основной продукт, которым мы пользуемся сегодня. А вот завтра станут более доступны факторы свёртывания (VIII фактор, в частности), ингибитор тромбопластина, антитромбин III, тканевой активатор плазминогена (алтеплаза), эритропоэтин. Также будет, надеемся, препарат, который сегодня используют для сокрытия следов проплывшей подводной лодки — вещество, аналогичное тому, которое покрывает тело рыбы, дельфина, кита — полиэтиленоксид. Его-то и взяли для эксперимента, о котором я говорил (когда из кроликов выливали кровь). Это, конечно, в будущем.
Сегодня при тяжёлом малокровии мы иногда вынуждены переливать эритроциты. Мы не можем обходиться без эритроцитов при остановке гемопоэза, при апластических анемиях. Мы вынуждены переливать их при шоке, осложняющем пернициозно-анемическую кому. Тем не менее, желательно не перехлёстывать. В острой кровопотере на первый план выходит нарушение свёртываемости. Острая массивная кровопотеря с ДВС-синдромом — удел реанимационных отделений, поэтому следует немедленно переводить больного в реанимацию. Поскольку акушеры сталкиваются с этим нечасто, нужно забирать таких больных, тогда и жизнь женщин будет спасена и не будет драм, которые сегодня разыгрываются. Подсчитано, что в России смерть родильниц в 8 раз превышает таковую в Европе. Это много. Можем ли мы её снизить? Запросто! Должен сказать, что коагулология в нашей стране (в самых хороших учреждениях, в институтских городах — Иваново, Ярославль, Самара) развита лучше, чем в Америке. Это связано с тем, что ДВС-синдром был впервые изучен в Москве, в СССР. Однако нам психологически сложно отойти от традиционных подходов и переливать не эритроциты, а плазму. Спасибо за внимание.
ВОПРОСЫ И ОТВЕТЫ
Вопрос. Какова должна быть цель самых первых реанимационных мероприятий при острой кровопотере?
Ответ. Удержать на минимуме АД и остановить кровь. Это достигается при помощи солевых растворов, гидроксиэтилкрахмала (замечательное средство, дольше держится в кровеносном русле). Альбумин — очень дорогой препарат и стоит на втором месте.
Вопрос. Можно ли останавливать кровотечение механически?
Ответ. У родильниц? Давайте будем точны — у родильниц не следует останавливать кровотечение механически. Если имеет место задержка участка плаценты, его убирают. Если же кровотечение — переливают плазму. Важно следить за центральным венозным давлением, поскольку если сначала налить больную растворами, а затем — плазмой, можно вызвать отёк лёгких. С плазмы начинают — не для поддержания объёма, а прежде всего для остановки кровотечения (вместо плазмы можно назначить криопреципитат — это синоним). При ранениях кровотечение останавливают хирургическим путём — другого не дано.
Вопрос. Что по-вашему лучше переливать бригаде скорой помощи, если нет свежезамороженной плазмы?
Ответ. Пожалуй, лучше не выезжать на вызов. Существуют определённые средства лечения, а если их нет, то мы не врачи. Если нет скальпеля и пинцета, как удалять аппендикс? Без плазмы бригада выезжать не может.
Вопрос. Как вы относитесь к прямым переливаниям крови детям разных возрастов, в том числе при септических заболеваниях?
Ответ. Я работал микропедиатром, правда, очень давно. Тогда такие переливания называли «мама-попа-терапия», потому что ребёнку внутримышечно вливали сцеженное молоко, а также материнскую кровь. Как объясняли — «для стимуляции». Я этим не занимался. Ни сепсис, ни какие нарушения иммунитета никакими переливаниями крови (ни внутримышечными, ни внутривенными) лечить нельзя — это бред. Сегодня существуют чистые препараты гамма-глобулина, которого в тысячи раз больше во флаконе, чем в шприце крови. Тёплая донорская кровь одинаково вредна и детям и взрослым, хотя дети с ней справляются легче — у них фибринолиз активнее и ДВС-синдром не развивается. Мы, к сожалению, вынуждены очень много переливать компонентов крови больным гемофилией. Найдётся ли хоть один больной гемофилией, которого не заразили гепатитом? Ни одного. Американцы заразили СПИДом 80% детей, больных гемофилией, японцы — тоже. Вот вам детские переливания. Есть, наконец, антибиотики, не справляетесь — переправляйте ребёнка туда, где условия лучше. Надо запомнить, что прямых переливаний вообще не существует. Прямое переливание — гениальная вещь, если бы оно было возможно. Вы переливаете кровь через короткий отрезок трубки, а уже вливаете не то, что взяли. Вы переливаете сгустки.
Вопрос. Ожидается ли какая-нибудь официальная информация по показаниям к использованию препаратов крови? В настоящий момент мы получаем свежую информацию по этой теме только от Свидетелей Иеговы. Хотелось бы получить какие-нибудь юридические указания Минздрава.
Ответ. Конечно же, юридический документ — это хорошо, но у меня нет юридического документа на любой случай, и я всё-таки жив. Целые республики избавились от этой глупости — переливания цельной крови (в Белоруссии — лет 15 назад, на Алтае — лет 20 назад, в учреждениях, которые мы курируем, — давным-давно). Все инструкции носят рекомендательный характер. Если вы знаете науку, знаете, что это вредно, то как вы можете выполнять глупую инструкцию? Наши пациенты пока не знают своих прав. Представьте ситуацию: погибает женщина, которой перелили цельную кровь, есть документы, которые говорят, что это вредно. Если подать в суд, в Америке, это будет стоит больнице миллионы долларов (правда, расплачивается страховая компания, но врач будет уволен и пойдёт работать в другое учреждение). Мы близки к этому.
Вопрос. Вы говорили о том, что большой процент плазмы заражён, есть ли какие-то препараты, которые позволяют заменить плазму? Ведутся ли работы в этой области?
Ответ. Конечно, работы ведутся. Во всём мире работы идут, но заменить плазму пока полностью не можем. В будущем, я думаю, мы уйдём от неё. Но пока нам приходится использовать свежезамороженную плазму (либо криопреципитат, что одно и то же) с известной степенью риска. К сожалению, плазма вредна, опасна, но заменить её сегодня нечем. Попытка обезопасить плазму от вирусов — термическая и детергентная её обработка. Но эта работа ещё не окончена.
4. КРОВОПОТЕРЯ И РЕГУЛЯЦИЯ КРОВООБРАЩЕНИЯ В ХИРУРГИИ
Академик РАМН Г. М. Соловьёв.
Отдел кардиохирургии ММА им. И. М. Сеченова, Москва, Россия.
Отдел кардиохирургии ММА им. И. М. Сеченова, Москва, Россия.
Проблема кровопотери актуальна всегда потому, что она сопровождает человека во все времена в его борьбе за жизнь в схватках с животными, в междоусобных войнах и, наконец, в цивилизованном обществе кровопотеря — постоянный спутник хирургических операций, ранений и травм военного и мирного времени. При этом встаёт не безынтересный вопрос: каков объём крови у человека, каков он в сравнении с животными, как на него влияют половые различия. Современная наука обладает более точными методами определения объёма крови, на которых мы остановимся ниже. Кровь как часть внутренней среды организма обеспечивает обмен веществ в нём. Чем выше потребности обмена, тем выше по отношению к тканям организма объём крови. По отношению к весу тела объём крови у взрослых мужчин составляет 7,5%, а у женщин — 6,5%. Интересно, что объём крови у животных также пропорционален уровню обмена. Так, у зайца он составляет 7,5% массы тела, а у кролика только 5%. На слайде представлено распределение крови в сосудистой системе. Как видно, большая половина её находится в венозной части системы кровообращения, четверть — в сердце и лёгких. В капиллярах же, где осуществляется обмен веществ, находится лишь 4% объёма крови. Кровь, как мы покажем ниже, является частью системы кровообращения. Состоит из двух частей: плазмы и глобулярной части. Тесно связана с сосудистым тонусом, скоростью кровотока, интенсивностью обмена в различных частях органов и тканях организма. Таким образом, кровь как часть системы кровообращения служит целям транспорта всех видов обмена в организме.
Соответственно основным составляющим крови — плазме и глобулярной части в современной науке имеют место определение объёма плазмы, участвующей в кровообращении, и объёма эритроцитов, как основной глобулярной составляющей. Существуют красочные и радиоизотопные методы определения объёма плазмы. При тех и других в соответствии со временем смешивания крови (в норме — 10 мин) определяется концентрация краски или меченного радиоактивным изотопом 135I глобулина плазмы крови. Соответствующие формулы дают возможность определить плазменный объём крови. Для определения эритроцитарного объёма крови в кровь вводятся эритроциты, меченные радиоактивным 51Cr. Методики определения плазменного и глобулярного объёма крови, достаточно сложны, требуют специальных знаний, аппаратуры, но достаточно широко освоены в современной клинике. Эти параметры объёма крови позволили выявить такой важный показатель кровообращения, как дефицит объёма крови по плазме и эритроцитам и сопоставить их с изменениями сосудистого тонуса, кровообращением в больших сосудах (система макроциркуляции) и в мелких тканевых сосудах и сосудах обмена (система микроциркуляции).
Прежде чем рассмотреть эти понятия, мы остановимся на видах кровопотери, которые имеют место при травме и хирургических операциях. Наиболее контролируемой является наружная кровопотеря, которую составляет кровь, излившаяся при ранении, удалённая отсосом из раны во время операции и пропитавшая салфетки и операционное бельё. В послеоперационном периоде к наружной кровопотере относится кровь, поступающая через дренажи. Помимо наружной кровопотери имеет место так называемая внутренняя кровопотеря — это кровь, оставшаяся в полостях, не дренированная в банку отсоса, а также кровь, пропитавшая ткани в области хирургических разрезов, закрытых переломов костей и в травматически размозжённых мягких тканях. Помимо этих явных признаков кровопотери мы различаем перемещение плазменного и глобулярного объёма крови в системе микроциркуляции. Мы имеем в виду обратимую и необратимую агрегацию форменных элементов крови — так называемый феномен сладжа, при котором эритроциты выходят из кровообращения, аккумулируясь в агрегаты диаметром до 300 мкм, которые закупоривают систему микроциркуляции, производя картину шока и гипоксию ткани. Эти изменения мы классифицируем как депонирование и секвестрацию крови. Эти процессы значительно влияют на определение объёма крови и её дефицита. Чем значительнее указанные нарушения микроциркуляции, тем больше дефицит объёма крови неучтённой наружной и внутренней кровопотери.
При рассмотрении процесса кровопотери во время хирургической операции и травмы и после неё, имея в виду обратимость нарушений в системе микроциркуляции агрегации эритроцитов и перехода плазменного компонента в ткани, возникает необходимость исследования объёма крови в динамике, которая ограничивается возможностями метода его определения — главным образом периодом выведения индикатора. Так или иначе, имея возможность определения объёма кровопотери при хирургических операциях, мы имеем возможность исследовать реакцию системы кровообращения на различные степени кровопотери и создать её классификацию. Кровопотеря — уменьшение внутрисосудистого объёма крови — сопровождается активацией симпатоадреналовой системы.
На первых порах при сокращении просвета вен, их ёмкостного отдела (крупные вены), кровь выжимается в общую систему кровообращения, при этом усиливается приток крови к сердцу (преднагрузка) и тем самым необходимый объёмный кровоток поддерживается на определённом уровне. Далее при увеличении кровопотери констриктивный эффект переходит на артериолы части тканей опорно-двигательного аппарата и кожи, которые выключаются из кровообращения. Клинически это проявляется в бледности кожных покровов. Прогрессирование кровопотери сохраняет сниженный объём кровообращения в жизненно важных органах при снижении сердечного выброса. Это называется централизацией кровообращения. Далее кровообращение снижается и в жизненно важных органах, что клинически проявляется картиной геморрагического шока.
На основании наших исследований объёма крови мы разработали классификацию кровопотери.
К первой степени мы относим дефицит объёма крови 10%. Эта стадия не сопровождается падением АД, не изменяется, а иногда несколько растёт венозное давление, имеет место небольшая тахикардия.
Ко второй степени мы относим увеличение дефицита объёма крови от 10 до 25%. При этом имеет место последовательное нарастание тахикардии, появление снижения венозного, а затем артериального давления.
К третьей степени мы относим дефицит объёма крови более 25%. На этой стадии возникает развёрнутая картина геморрагического шока со снижением систолического давления ниже 80 мм рт.ст., тахикардией выше 120 уд/мин, низкими цифрами венозного давления в пределах 30–50 мм вод.ст.
Быстрая кровопотеря более 40% объёма крови приводит к остановке кровообращения и несовместима с жизнью. Эти цифры приблизительны и зависят от исходной гиповолемии и анемии, а также от толерантности к кровопотере, что связано с компенсаторными возможностями организма.
Хирурги нередко преувеличивают размеры кровопотери, называя цифры 3 л крови и более, что является следствием неточного измерения, смешивания крови с жидкостями и эмоциональным отношением к трагедии массивной кровопотери.
Говоря о внутренней кровопотере, мы выделили понятия депонирования и секвестрации крови вследствие феномена сладжа, который появляется при гипоксии тканей как реакция на кровопотерю. Механизмы возникновения агрегации эритроцитов достаточно сложны, но факторы, приводящие к сладжу, в значительной мере изучены, они многогранны. Мы исследовали нарушение кровообращения в системе микроциркуляции при кровопотере, во время искусственного кровообращения (ИК), которое во многом воспроизводит геморрагический шок, динамическим микрофотографированием бульбарной конъюнктивы больного.
Эти исследования также показали различные степени нарушений микроциркуляции, условно трёх степеней:
при первой — агрегация в капиллярах и малых венулах диаметром менее 30 мкм;
при второй — капилляров не видно, агрегация в венулах 35–100 мкм, артериолы спазмированы;
при третьей — агрегация в крупных венулах до 100 мкм и более и в артериолах. Непрерывный кровоток в сосудах микроциркуляции отсутствует.
Агрегация эритроцитов — состояние обратимое и при изменении тонуса сосудов, изменении белкового состояния плазмы, а также при введении антиагрегантов в кровеносное русло она уменьшается или исчезает. Необратимую агрегацию, сопровождающуюся тяжёлыми изменениями в тканях — их гипоксическим повреждением вследствие резкой кровопотери, мы называем секвестрацией крови. Секвестрация крови сопровождает клиническую картину полиорганной недостаточности и является составной частью распространённого внутрисосудистого свёртывания (РВС или ДВС).
Насколько микроциркуляция автономна, показывает отсутствие параллелей между степенью агрегации эритроцитов и показателями кровообращения в системе макроциркуляции. Как мы уже указывали выше, организм на кровопотерю реагирует активацией симпатоадреналовой системы. Содержание катехоламинов в крови при кровопотере со снижением артериального давления может увеличиваться в 100 и более раз. Этот спазм обусловлен деятельностью барорецепторов. Помимо катехоламинов возрастает выброс альдостерона и глюкокортикоидов. Посткапиллярное сопротивление повышается меньше, чем прекапиллярное, что обусловливает при продолжающемся кровотечении переход жидкости из тканей в кровь и поддержание объёма крови её разведением.
К первой фазе вазоконстрикции можно отнести сужение ёмкостного отдела вен, а затем тканей кожи и мышц, что является компенсаторной реакцией — централизация кровообращения, не приводящая к повреждению органов. Вторая фаза направлена на поддержание артериального давления, но приводит к их повреждению — фаза декомпенсации микроциркуляции, закупорка агрегатами входа в её систему и шунтирование крови по артерио-венозным шунтам в обход капиллярной сети.
Переливание крови как метод лечения кровопотери широко обсуждается в литературе последних двух десятилетий. Здесь нет однозначных решений. Сегодня является очевидным отсутствие необходимости переливания крови при кровопотере первой степени до 10% объёма крови. Это, как правило, обычные полостные хирургические операции, включая резекцию желудка.
Во-вторых, доказана нежелательность переливания цельной консервированной крови. Помимо того, что к 10–12-му дню она вызывает иммунный ответ, нами показано, что к 5-му дню хранения в ней исчезают все биологически активные вещества, имеет место закисление крови, увеличивается количество калия и возникает ряд других изменений. Причём эти явления имеют место до появления заметного гемолиза. Начиная с 5-го дня после переливания крови её эритроциты начинают разрушаться, стимулируя гемопоэз собственных клеток крови.
Особое место в проблеме переливания крови имеют место операции на сердце в условиях ИК, когда нередко в АИК приходится заливать препараты крови (отмытые размороженные эритроциты). Операция проходит в условиях искусственной гемодилюции, которая частично остаётся и в послеоперационном периоде, что обусловливает значительную послеоперационную кровопотерю. Эту проблему мы обсудим в отдельном сообщении, а в конце данного сообщения нам хотелось бы остановиться на массивных переливаниях крови при массивной кровопотере. В данном случае переливание крови может выглядеть как пересадка ткани с иммунологическим ответом на неё. Однако массивное переливание консервированной крови и её препаратов обусловлено массивной кровопотерей, которая, как мы показали выше, сопровождается декомпенсацией кровообращения в системе микроциркуляции с повреждением тканей жизненно важных органов с последующей полиорганной недостаточностью. Проявления органной недостаточности, например шоковое лёгкое, шоковая почка, могут быть связаны с шунтированием крови и с нарушением микроциркуляции в органах.
Проблема кровопотери в хирургии остаётся актуальной и сегодня. Остаётся актуальным вопрос — стоит ли определять кровопотерю во время операции, так как мы в основном ориентируемся на наружную кровопотерю, но не знаем дооперационный объём крови больного, не можем количественно учитывать феноменов депонирования и секвестрации крови. В этих условиях хирурги и анестезиологи, как правило, недооценивают кровопотерю даже при учёте всех клинически проявляющихся механизмов компенсации кровообращения в ответ на кровопотерю.
Это сообщение стало возможным благодаря нашим исследованиям и исследованиям моих учеников и сотрудников, выполненным в конце 60-х и 70-е гг. Это диссертационные работы М. Л. Ходас, И. Я. Усватовой, Г. Х. Пятницкой, М. Н. Иванникова, Г. Г. Радзивила, В. В. Гуденко, А. В. Мещерякова, Е. П. Смирнова, К. М. Шульмана и ряд статей последующих лет. Основные материалы изложены в нашей монографии «Кровопотеря и регуляция кровообращения в хирургии», которая, как нам кажется, не устарела и сегодня.
5. ПРИМЕНЕНИЕ ИНФУКОЛА ДЛЯ КОРРЕКЦИИ ГИПОВОЛЕМИИ В ИНТРАОПЕРАЦИОННОМ ПЕРИОДЕ
А. В. Бутров, С. Г. Цимбалов, В. И. Морозов, И. А. Олийниченко.
Кафедра анестезиологии и реаниматологии Российского университета дружбы народов, Москва, Россия.
Кафедра анестезиологии и реаниматологии Российского университета дружбы народов, Москва, Россия.
Гиповолемия является наиболее частым синдромным нарушением в интраоперационном периоде. Поэтому изучение инфузионных сред для волемической поддержки и коррекции гиповолемии всегда будет актуальным. Повышенный интерес к инфузионной терапии связан также с достаточным разнообразием объёмозамещающих средств, имеющих комплексное влияние на гемостаз.
Исследование проведено у 24 гинекологических больных, которым произведена экстирпация матки. Общая интраоперационная кровопотеря составила от 10 до 15% ОЦК. Гемотрансфузию не проводили. У всех больных использовали одинаковый режим инфузионной терапии: физиологический раствор 1200 мл, 5% раствор глюкозы 400 мл. Гидроксиэтилкрахмал (ГЭК) — ИНФУКОЛ 6%, 200/0,5 фирмы «ЗЕРУМ-БЕРК БЕРНБУРГ АГ» использовали в объёме 500 мл с целью коррекции интраоперационной гиповолемии.
Все больные оперированы под эндотрахеальным наркозом, в условиях нейролептанальгезии (фентанил, дроперидол) и миоплегии (павулон, ардуан).
Мониторировали: систолическое артериальное давление (АДсист), диастолическое артериальное давление (АДд), среднее артериальное давление (САД), частоту сердечных сокращений (ЧСС), сатурацию (пульс-оксиметрия). Центральное венозное давление (ЦВД) измеряли аппаратом Вальдмана, сердечный индекс (СИ) — методом тетраполярной реографии аппаратом «Рео-1». Индекс общего периферического сопротивления (ИОПС) рассчитывали по стандартной формуле.
Учитывая фармакодинамику гидроксиэтилкрахмала, анализ параметров гемодинамики проводили на трёх этапах: 1-й этап — до переливания ГЭК, 2-й этап — через 30 мин после переливания ГЭК, 3-й этап — через 4 ч после переливания ГЭК.
Исследовали следующие лабораторные показатели: гемоглобин (Hb), гематокрит (Hct), эритроциты, тромбоциты, общий белок плазмы, амилазу. Биохимические показатели также анализировали на трёх этапах, но с отличным (по отношению к анализу гемодинамики) интервалом времени: 1-й этап — до переливания ГЭК, 2-й этап — 4 ч после переливания ГЭК, 3-й этап — 12 ч после переливания ГЭК.
Из параметров коагулограммы исследовали и анализировали концентрацию фибриногена в плазме, активированное частичное тромбопластиновое время (АЧТВ), протромбиновое время (ПВ), время кровотечения (ВК) на двух этапах: до переливания ГЭК и через 1 сут после переливания ГЭК.
Статистическая обработка проведена по t критерию Стьюдента.
Результаты исследования представлены тремя блоками линейных графиков. На каждом графике представлены в цифровом формате среднее арифметическое выборки и в графическом формате стандартное отклонение.
При анализе изменения гемодинамики (график 1) отмечено прогрессивное увеличение САД (9,1%; 17,9% — здесь и далее процентное отношение последующих этапов исследования по отношению к исходному этапу — до переливания ГЭК, p<0,01), ЦВД (105,6%; 161%, p<0,01), достоверное снижение ЧСС (−11,3%; −19,3%, p<0,01). СИ повышался через 30 мин после переливания ГЭК на 10,5% (p<0,01) и снижался до исходного уровня через 4 ч после переливания ГЭК. ИОПС (для графической читабельности представлен в условных единицах измерения) снижался на 10,4% (p<0,05) через 30 мин после окончания инфузии ГЭК и восстанавливался до исходного уровня через 4 ч.
Динамика лабораторных показателей (график 2) носит характер тенденций, за исключением прогрессивного увеличения концентрации амилазы (88,2%; 146,3%, p<0,01). Из остальных лабораторных показателей через 30 мин после окончания переливания ГЭК отмечено снижение Hb (−6,7%, p<0,05) и эритроцитов (−10,1%, p<0,05).
Из параметров коагулограммы (график 3) динамически изменялся только протромбиновый индекс (28,4%, p<0,01). Увеличение времени кровотечения недостоверно, фибриноген и АЧТВ оставались без изменения.
Полученный нами гемодинамический профиль на исходном этапе исследования (по переливанию ГЭК) полностью соответствует гиповолемическому состоянию: недостаточная преднагрузка, сниженный сердечный выброс, и как компенсация первых двух параметров, повышение ИОПС [5:1][5:2]. Эти данные (график 1) не соответствуют состоянию шока, то есть декомпенсации тканевого обмена, но предполагают высокую вероятность развития последнего без адекватной коррекции [5:3][5:4].
Основная цель терапии при гиповолемии — увеличение объёма циркулирующей крови (ОЦК) и преднагрузки [5:4]. С целью коррекции ОЦК в условиях интраоперационной кровопотери мы применили ГЭК. Гемодинамический профиль (график 1) через 30 мин после переливания ГЭК показывает адекватную коррекцию преднагрузки и восполнение ОЦК. Такую быструю стабилизацию мы связываем с терапевтической эффективностью ГЭК, которая выражается в объёмозамещающем действии, то есть способностью удерживать и связывать воду в состоянии циркулирующей жидкости [5:1]. По фармакодинамике ГЭК данный эффект сопровождается 4 ч [5:5], поэтому следующим этапом анализа гемодинамики мы выбрали временной интервал 4 ч после окончания инфузии. Несмотря на снижение объёмозамещающего эффекта ГЭК, продолжается дальнейшая стабилизация гемодинамики, что выражается в прогрессивном увеличении перфузионного давления, нормализации преднагрузки (САД, ЦВД, график 1). Возвращение СИ и ИОПС к исходному состоянию вызвано перераспределением кровотока. Но в отличие от исходного состояния, за счёт устранения тахикардии и адекватного перфузионного давления, на данном этапе сократительная способность миокарда выше, а главное, увеличен резерв ударного объёма к компенсации за счёт улучшения диастолического наполнения желудочков.
Анализ лабораторных показателей не выявил выраженного эффекта гемодилюции (график 2). Незначительное снижение Hb и Hct, более выраженное — эритроцитов, без существенного снижения белка и разведения тромбоцитов предполагает, что использованный объём ГЭК (500 мл) вызывает не столько гемодилюцию, сколько мобилизацию форменных элементов крови из физиологического депонирования и вовлечение последних в активную циркуляцию. Увеличение амилазы в 2,5 раза (график 2) находится в пределе заданного уровня устойчивости к действию амилаз сыворотки крови для ГЭК [5:6].
Применение ГЭК в нашем исследовании не выявило никаких изменений в системе гемостаза. Увеличение протромбинового времени (график 3), несмотря на его достоверность, в отсутствие изменений других параметров коагулограммы однозначного обоснования не имеет. Кроме того, эти изменения находятся в интервале нормы.
Применение Инфукола 6%, 200/0,5 — производного ГЭК — в условиях интраоперационной гиповолемии быстро стабилизирует гемодинамику, эффективно восстанавливает объём циркулирующей крови, препятствует развитию гиповолемического шока. Инфукол 6%, 200/0,5 в дозе 500 мл при коррекции гиповолемии не приводит к выраженной гемодилюции и не оказывает отрицательного влияния на состояние гемостаза.
1 — до переливания;
2 — 30 минут после переливания;
3 — 4 часа после переливания.
График 2. Изменение лабораторных показателей в зависимости от переливания Инфукола 6% — 200/0,5.
Ось X — этапы исследования: 1 — до переливания; 2 — 4 часа после переливания; 3 — 12 часов после переливания.
|
График 3. Изменение коагулограммы в зависимости от переливания Инфукола 6%, 200/0,5.
Ось X — этапы исследования: 1 — до переливания; 2 — 1-е сутки после переливания.
|
ЛИТЕРАТУРА
- [5:1] Shatney C. H., Deepika K., Militello R. P., et al. Arch. Surg. 1986; 118:104.
- [5:2] Shoemaker W. C., Appel P. L., Kram H. B. Chest 1993; 102:209.
- [5:3] Rackow E. C., Falk J. L., Fein I. A., et al. Crit. Care Med. 1983; 11:839–850.
- [5:4] Shoemaker W. C., Fleming A. W. Ann. Emerg. Med. 1986, 12:1437–1444.
- [5:5] Молчанов И. В., Гольдина О. А., Горбачевский Ю. В. Растворы гидроксиэтилированного крахмала — современные и эффективные плазмозамещающие средства. Монографический обзор, Москва, 1998.
- [5:6] Condit D., Freeman K., Brodman R. J. Crit. Care 1987; 2:36–38.
6. ОПЫТ АУТОДОНОРСТВА И СБЕРЕЖЕНИЯ КРОВИ В СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ
Г. М. Соловьёв, Л. В. Попов, С. П. Наумов, А. А. Силаев, М. В. Супрунов.
Отдел кардиохирургии ММА им. И. М. Сеченова, Москва, Россия.
Отдел кардиохирургии ММА им. И. М. Сеченова, Москва, Россия.
В данном сообщении мы рассматриваем проблемы кровопотери, переливания крови и регуляции кровообращения в связи с операциями на сердце в условиях искусственного кровообращения (ИК).
Сам термин ИК не точен, в указанных условиях имеет место не ИК, а перфузия организма перфузатом, состоящим из кровезаменителей и консервированной крови, в резко антифизиологических условиях, при которых нарушены все параметры кровообращения и в считанные минуты меняется вся внутренняя среда организма. При ИК значительно меняются параметры макроциркуляции, артериальное и венозное давление, происходит перераспределение объёма крови.
Под влиянием активации симпатоадреналовой системы перераспределяется и изменяется кровенаполнение органов, меняется сосудистый тонус, возникают нарушения в системе микроциркуляции, происходит так называемая централизация кровообращения, при которой организм для самосохранения переносит акцент на поддержание жизнедеятельности внутренних органов, ядра организма, жертвуя кровоснабжением опорно-двигательного аппарата и кожи — плаща организма.
Мы имеем возможность сравнивать состояние организма при ИК с клинической картиной шока. Во время операции на сердце при ИК образуется перераспределение крови между кровообращением больного и системой заполнения аппарата. Часть крови больного в разведении перфузатом перемещается в аппарат ИК, ёмкость которого варьирует в зависимости от применяемой системы до 2 л крови.
Таким образом, организм при ИК теряет кровь, происходит как бы кровотечение в аппарат. Естественно, организм больного не может не реагировать на эту кровопотерю, которая накладывается на дезорганизацию регуляции кровообращения и внутренней среды организма в связи с возникшими условиями. Ситуация достаточно трагичная, она вызывает перенапряжение всех систем регуляции организма. Именно поэтому пациент с трудом переносит ИК, которое длится более 3–4 ч. Патологические сдвиги, возникающие при этом, приводят к гибели больного. Однако современная анестезиология и перфузионные среды позволяют проводить ИК в течение указанного времени. ИК как неизбежность необходимо для выключения сердца и производства операций на нём.
Консервированная кровь, использованная в указанных операциях, дополняет перечень отрицательных факторов, влияющих на организм. Вредное влияние консервированной крови было установлено в литературе и многочисленных наших исследованиях в конце 60-х и 70-х гг. Конечным результатом этого влияния является нарушение в системе микроциркуляции, уже имеющее место в связи с проведением ИК. Поэтому методика ИК последовательно ушла от заполнения аппарата цельной кровью, перейдя к заполнению кровезаменителями, входящими в состав перфузата.
Переливание чужеродной крови и её препаратов отрицательно сказывается и в послеоперационном периоде, вызывая иммунный ответ организма, а также развитие анемии в связи с гибелью чужеродных консервированных эритроцитов.
Современная техника ИК и анестезия позволяют избегать переливания чужеродной консервированной крови, во всяком случае, у тех больных, у которых не возникают значительные послеоперационные кровотечения.
В настоящее время отмечается тенденция к ограничению и полному отказу от использования донорской крови во время операций на сердце с применением ИК. Это стало возможным в связи с тем, что современные оксигенаторы и системы для проведения ИК требуют малого объёма заполнения, а снижение кислородной ёмкости крови, связанное с применением кровезаменителей, для заполнения системы, не снижает транспорт кислорода до критических величин.
Возникающая при этом гемодилюция уменьшает травматизацию крови и агрегацию форменных элементов крови, улучшая тем самым микроциркуляцию.
Во время операции, при доступе к сердцу и после введения протамина сульфата имеет место кровотечение в салфетки и отсос. В последние годы отмечается увеличение внимания к использованию аутокрови у кардиохирургических больных. Это также связано с тем, что в настоящее время резко сократилось донорство.
Заготовка аутокрови, или эксфузия, имеет три разновидности:
(а) однократная эксфузия за 3–5 дней до операции с объёмом 250–400 мл,
(б) ступенчатая эксфузия проводится несколько раз (2–4 раза) с интервалом 3–5–7 дней с возмещением объёма кровопотери коллоидными и кристаллоидными кровезаменителями с сохранением аутокрови в банке крови,
(в) эксфузия аутокрови проводится на операционном столе во время операции на начальном этапе ИК.
17 В своей работе мы использовали третий способ забора крови. Аппарат ИК заполняли кристаллоидными растворами, проводили коррекцию электролитного состава перфузата. Канюляция нижней и верхней полых вен проводилась по стандартной методике. Из общей магистрали, по которой кровь поступает в аппарат ИК, с помощью выпускника на начальном этапе параллельного ИК производили забор (эксфузию) крови стерильными флаконами.
Объём крови для эксфузии определяли исходя из объёма циркулирующей крови (ОЦК), который рассчитывали по номограмме фирмы ТРАВЕНОЛ исходя из показателей гемоглобина, гематокрита, веса, роста, поверхности тела больного.
По окончании ИК, стабилизации гемодинамики больному переливали оставшийся объём так называемой аппаратной крови, содержащей гепарин. Нейтрализацию гепарина проводили протамина сульфатом.
При недостаточном диурезе во время ИК вводили диуретики (лазикс) с целью повышения гемоконцентрации.
Возврат больному аутокрови начинали на этапе окончательного свёртывания крови и получения сгустков. Если весь объём аутокрови не удавалось ввести после окончания ИК, то оставшийся объём вводили в отделении реанимации.
Мы проанализировали результаты 425 оперированных больных с приобретёнными пороками сердца, которым произведён забор аутокрови и не производилось интраоперационное переливание донорской крови.
Все больные разделены на три группы.
| Группа | Кол-во больных | В/в Hb до ИК, г/л | Hb ИК, г/л | Эксфузия, мл | Кровопотеря, мл |
|---|---|---|---|---|---|
1-я ИБС
|
95
|
145–168 ср. 132
|
6,5–9,5
|
500–1250 ср. 875
|
120–225 ср. 162
|
2-я МК
|
214
|
119–142 ср. 126
|
72–93
|
350–1200 ср. 480
|
320–410 ср. 394
|
3-я АК
|
116
|
117–163 ср. 143
|
82–92
|
400–1200 ср. 650
|
250–370 ср. 318
|
Основываясь на нашем опыте, можно сказать, что предварительно рассчитанная эксфузия крови приводит к снижению гемоглобина крови, но не нарушает транспорт кислорода во время ИК. Второе, эксфузия и последующие вливания крови не вызывают резких изменений в системе геморегуляции. Третье, использование аутокрови позволяет значительно снизить количественную потребность в донорской крови или вообще её не использовать.
Таким образом, ИК с переливанием аутокрови позволило сохранить обычные параметры кровообращения во время ИК, адекватное восстановление гемодинамики после ИК и операции, а также нормализацию гемоконцентрационных показателей у больных. Более того, в анализируемой группе больных отсутствовал гемолиз крови в аппарате. Однако удлинение показателей свёртываемости крови в конце и после операции, как правило, имеет место, поэтому средняя кровопотеря по дренажам составляет 500–600 мл, что иногда требует переливания донорской крови.
Для операции на сердце, как правило, используется универсальный доступ — продольная стернотомия, во время которой отмечается заметное кровотечение из губчатого вещества грудины. Предложенное для его остановки промазывание грудины воском малоэффективно и связано с наличием инородного тела в разрезе сшитой в конце операции грудины, а тщательная электрокоагуляция костной ткани и надкостницы также нежелательна в связи с отрицательным влиянием на репаративный процесс.
В последнее время в нашей клинике широко используется биологический фибриновый клей, который изготавливается на нашей станции переливания крови по собственному рецепту.
Клей состоит из двух ингредиентов — фибриногена и тромбина с кальцием. При смешивании этих двух частей образовывалась фибриновая плёнка, которая не требовала сухого поля благодаря пропитыванию кровоточащей поверхности. Этот метод остановки кровотечения мы применили в кардиохирургии, в частности для гемостаза распила грудины в момент её сшивания. Для этого обычную гемостатическую губку пропитывали фибриновым клеем и прокладывали её в разрез сшиваемой грудины. Также клей применяли с целью герметизации швов левого предсердия, аорты, коронарных анастомозов при аортокоронарном шунтировании. При данных вмешательствах, несмотря на удлинение показателей свёртываемости в послеоперационном периоде, кровопотеря сократилась в 1,5–2 раза. Во всех случаях не было отмечено значительного кровотечения и ни разу не была предпринята рестернотомия для остановки кровотечения.
Таким образом, внедрение методов остановки кровотечения при применении фибринового клея уменьшает кровопотерю и наряду с аутотрансфузией во время ИК позволяет избежать переливания чужеродной донорской крови.
7. ОПЫТ ПРОВЕДЕНИЯ БЕСКРОВНЫХ ОПЕРАЦИЙ НА ОТКРЫТОМ СЕРДЦЕ
А. Н. Корниенко, В. И. Иванченко, А. Г. Киртаев, И. В. Кузнецов, М. И. Шуварин, А. А. Пайвин, К. Ю. Малыгин.
Центральный военный клинический госпиталь им. А. А. Вишневского, Москва, Россия.
Центральный военный клинический госпиталь им. А. А. Вишневского, Москва, Россия.
Операции на сердце в условиях искусственного кровообращения (ИК) сопровождаются повышенной кровоточивостью и нередко требуют переливания донорской крови. Для уменьшения использования донорской крови традиционно применяются:
— предоперационная заготовка аутокрови;
— интраоперационная реинфузия аутокрови с помощью аппарата Cell Saver;
— гемодилюция.
С 1994 г. в кардиохирургическом центре Центрального военного клинического госпиталя им. А. А. Вишневского стали внедряться вышеперечисленные методики. За этот период выполнено более 600 операций на сердце в условиях ИК. В 1994–1996 гг. использовалась методика нормоволемической гемодилюции в сочетании с предоперационной заготовкой аутоплазмы. Плазма заготавливалась методом плазмафереза в течение 7–10 дней перед операцией.
Непосредственно на операционном столе осуществляли острую нормоволемическую гемодилюцию. Кровь забирали в доперфузионном периоде до введения гепарина в объёме 500–800 мл с одновременным замещением теряемого объёма коллоидно-кристаллоидными растворами. Однако данная методика таит в себе риск развития неуправляемой гемодилюции с разведением крови в ходе ИК до гематокрита менее 20%. Это происходит вследствие применения кристаллоидной кардиоплегии, особенно при длительных операциях с ИК до 2 ч и более, что требует использования ультрафильтрации перфузата.
Аппарат Cell Saver интраоперационно использовали в 1994 г. при небольшом количестве (8) операций и в дальнейшем вынуждены были отказаться от данной методики вследствие её высокой стоимости, а также благодаря эффективному использованию реинфузии аутокрови из раны через оксигенатор аппарата ИК. Позднее, с 1995 г., при кардиохирургических вмешательствах была разработана методика анестезии с применением высокой эпидуральной блокады, что кроме повышения эффективности анальгезии позволило применить острую гиперволемическую гемодилюцию без риска увеличения пред- и постнагрузки миокарда. Таким образом, мы полностью отказались от эксфузии аутокрови.
В 1996 г. была внедрена методика озонирования крови в оксигенаторе, которая первоначально преследовала цель иммунокоррекции у больных с септическим эндокардитом. Однако в дальнейшем кроме повышения кислородотранспортной функции крови было обнаружено, что озон уменьшает повреждающее действие ИК на организм. Отмечено снижение уровня лактата в крови, уменьшение числа патологически изменённых и деструктивных форм эритроцитов. При этом озон не активировал процессы перекисного окисления липидов и умеренно стимулировал активность антиоксидантной системы. Переход к нормотермической перфузии способствовал снижению случаев развития гипотермической коагулопатии и сократил длительность ИК в среднем на 18,8%.
В этом же году внедрение кровяной кардиоплегии решило проблему развития неуправляемой гемодилюции во время длительного ИК. Так, если при традиционной кристаллоидной кардиоплегии в сочетании с наружным охлаждением за 1 ч ИК вводилось от 1200 до 1800 мл растворов, то при кровяной кардиоплегии за 1 ч ИК расходовалось не более 300 мл кристаллоидных растворов, при этом наружное охлаждение миокарда не проводилось и не применялись утильные отсосы. Кроме того, кровяная, а в дальнейшем озонированная кровяная кардиоплегия позволила повысить эффективность защиты миокарда, что проявилось улучшением кардиогемодинамики в постишемическом периоде, быстрым и эффективным восстановлением биоэлектрической и сократительной функции сердца, повышением сердечного индекса, улучшением доставки кислорода тканям, уменьшением дозы и длительности инотропной стимуляции миокарда в послеоперационном периоде.
Так, при операциях АКШ при озонированной кровяной кардиоплегии самостоятельное восстановление сердечного ритма зафиксировано в 92,3% наблюдений, в отличие от кристаллоидной, где самостоятельное восстановление сердечной деятельности отмечалось лишь в 66,6% (p<0,05). Частота использования инотропной поддержки дофамином в ближайшем постперфузионном периоде при использовании кровяной кардиоплегии составила 12,6% и при кристаллоидной — 46,6% (p<0,05).
Известно, что состояние системы гемостаза зависит не только от степени гемодилюции, травматичности операции, длительности ИК, но и от типа оксигенатора и методики применения антикоагулянтов и прокоагулянтов. Методика перфузии была следующей. Экстракорпоральное кровообращение проводилось с применением гиперволемической гемодилюции, нормотермической перфузии, кровяной озонированной холодовой кардиоплегии и озонирования крови в контуре аппарата ИК. Объёмная скорость перфузии составила 2,4–2,6 л/м2.
В доперфузионный период на фоне развития эпидуральной блокады и вазоплегии осуществляли инфузионную терапию в объёме 1468±23 мл. Применялась холодовая кровяная кардиоплегия в соотношении крови к кардиоплегическому раствору 4:1 с декомпрессией левого желудочка без наружного охлаждения миокарда. При перфузии осуществлялась озонация крови в течение всего сеанса ИК путём подачи в оксигенатор кислородно-озоновой смеси с содержанием озона 8–10 мкг/л/мин и общей дозой вводимого озона до 2000 мкг.
Операции выполнены с использованием аппарата искусственного кровообращения фирмы «Stokert» (Германия), одноразовых пузырьковых оксигенаторов фирмы «Dideco» (Италия) и мембранных оксигенаторов фирмы «Baxter» (США). В настоящее время предпочтение отдано мембранным оксигенаторам.
Методика управляемой гипокоагуляции была стандартная. Перед ИК вводили гепарин в дозе 3 мг/кг под контролем активированного времени свёртывания крови. В оксигенатор добавляли гепарин в дозе 50 мг/л перфузата и в последующем по 50 мг каждый час ИК. Нейтрализацию гепарина осуществляли капельным внутривенным введением протамина сульфата в дозе соответственно введённому гепарину 1:1 в течение 5–10 мин в разведении на 200 мл эпсилон-аминокапроновой кислоты. Дополнительно применялись ингибиторы протеолитических ферментов и активаторы агрегации тромбоцитов. От применения последних отказались с 1996 г. вследствие сомнительной их эффективности. Практически у всех больных в послеоперационном периоде отмечалось снижение факторов свёртывания как первичного, так и вторичного гемостаза, активация фибринолиза. Однако только при наличии клинических признаков кровотечения в послеоперационном периоде использовали донорскую плазму, криопреципитат и тромбовзвесь. Исходя из опыта, пришли к выводу, что кровотечение по дренажам в течение первых 3 ч со скоростью 100 мл/ч и более требует срочной рестернотомии. Консервативные мероприятия, как правило, только приводят к потере времени и увеличению кровопотери. Интересен факт, что при рестернотомии в одной трети случаев явных источников кровотечения не найдено, однако кровотечение прекращалось. Существенным фактором обеспечения надёжного гемостаза в постперфузионном периоде явилось применение новых аппаратов диатермокоагуляции типа «Valeylabb» с выполнением тщательного хирургического гемостаза как на доперфузионном этапе операции, так и после ИК.
На сегодняшний день кровопотеря за первые сутки послеоперационного периода по дренажам при АКШ в нашей клинике составляет в среднем 254 мл, при коррекции приобретённых пороков — 478 мл, при коррекции врождённых пороков — 185 мл. Количество рестернотомий, связанных с кровотечением, снизилось с 12,3% в 1996 г. до 3,5% в 1998 г.
Благодаря комплексному использованию современных методов хирургической техники и анестезиологического обеспечения удалось снизить частоту применения донорской крови и её компонентов. Так, средний расход эритроцитарной массы снизился с 593 мл/чел в 1995 г. до 54,8 мл/чел — в 1998 г., свежезамороженной плазмы — с 620 до 130 мл/чел, альбумина — с 120,3 до 12,0 мл/чел соответственно. Переливание крови или её компонентов в 1998 г. потребовалось при операциях АКШ в 11,7% случаев и в 38,6% при операциях коррекции пороков сердца. Более высокий процент случаев переливания донорской крови и её препаратов у больных с пороками сердца обусловлен часто имеющейся исходной анемией, сепсисом и явлениями полиорганной недостаточности. В целом летальность с 18,4% в 1993 г. снизилась до 1,9% — в 1998.
Таким образом, на современном этапе развития кардиохирургии и анестезиологии при операциях АКШ возможно полностью отказаться от применения донорской крови и её компонентов, а при операциях коррекции пороков существенно сократить путём:
— выполнения тщательного хирургического гемостаза с использованием современных аппаратов диатермокоагуляции;
— применения гиперволемической гемодилюции;
— нормотермической перфузии;
— кровяной кардиоплегии;
— использования оксигенаторов мембранного типа.
8. ОСОБЕННОСТИ ИНТРАОПЕРАЦИОННОГО ОБЕСПЕЧЕНИЯ БЕСКРОВНОЙ ХИРУРГИИ У БОЛЬНЫХ ИБС
Н. А. Трекова, А. Г. Яворовский, Б. В. Шабалкин, А. Г. Кротовский, М. А. Чарная, М. М. Шмырин, С. В. Ванина, Г. А. Рагимов, И. А. Крапивкин.
Научный центр хирургии РАМН, Москва, Россия.
Научный центр хирургии РАМН, Москва, Россия.
Кровотечение является одним из самых тяжёлых осложнений, возникающих при кардиохирургических операциях с ИК, и может привести к нарушению различных звеньев гомеостаза организма, а именно — к нарушению свёртывающей системы крови, к нарушению кислороднотранспортной функции крови и к гиповолемии. С другой стороны, переливание донорской крови с целью коррекции этих нарушений может сопровождаться развитием синдрома гомологичной крови, приводить к развитию аллергических реакций, а также к различным инфекционным заболеваниям. В этой связи весьма актуальной является задача разработки мер, позволяющих создать условия для бескровной хирургии.
С нашей точки зрения, для реализации бескровной хирургии (речь ведётся о хирургии ИБС) необходимо обеспечить следующий комплекс интраоперационных мер:
(1) Профилактика и лечение интраоперационной гипертензии.
(2) Умеренная гемодилюция в предперфузионном периоде.
(3) Управляемый (форсированный) диурез.
(4) Гемофильтрация.
(5) Использование больших доз трасилола.
Остановимся более подробно на каждом из перечисленных положений.
(1) Профилактика и лечение интраоперационной гипертензии.
Как показали наши исследования, наибольшей кровопотерей, особенно на фоне гипертензии, сопровождаются следующие этапы операции: стернотомия, выделение внутренней грудной артерии, канюляция аорты. Кроме того, необходимо учитывать, что при операциях по поводу ИБС мы имеем дело с довольно большой раневой поверхностью (одновременно на нижних конечностях — выделение вены, верхних конечностях — выделение лучевой артерии и грудной клетке). И естественно, объём кровопотери в такой ситуации может быть повышен, особенно на фоне артериальной гипертензии. Так, объём кровопотери в доперфузионном периоде у больных без артериальной гипертензии составил 125±27 мл, а у пациентов с артериальной гипертензией 215±19 мл (p<0,05). В этой связи чрезвычайно важно обеспечить управляемую умеренную гипотонию, и особенно на этапах операции, указанных выше.
С этой целью мы используем: периферические вазодилятаторы (нитропруссид Na, нитроглицерин), блокаторы кальциевых канальцев (нифедипин, исрадипин), ингаляционные анестетики (фторотан, изофлюран), β-блокаторы (эсмолол).
Одним из основных требований к препаратам, используемых для профилактики и коррекции артериальной гипертензии, является их управляемость. В этом смысле препаратом выбора является нитропруссид Na, затем эсмолол, изофлюран, исрадипин и, пожалуй, наименее управляемым является нифедипин.
(2) Умеренная гемодилюция в предперфузионном периоде.
Под этим мы подразумеваем эксфузию 400 мл крови на этапе до ИК и замещение её 1:2 коллоидными и кристаллоидными растворами. Эксфузией крови мы преследуем три цели:
— достижение искусственной гемодилюции, что уменьшает объём теряемых эритроцитов в предперфузионном и перфузионном периодах;
— восполнение ОЦК при инфузии аутокрови в постперфузионном периоде;
— восстановление свёртывающей системы крови.
Эксфузию крови осуществляли у 31% больных, после чего уровень Ht снижался в среднем на 17% и перед началом ИК составлял 34±2%, тогда как в группе пациентов без эксфузии крови (II гр.) величина Ht была 39±3%. Несмотря на достоверную разницу в уровне Ht, между этими группами в конце ИК величины Ht в обеих группах были одинаковыми, а на этапе гемостаза уровень Ht во II группе был достоверно ниже — 27±3%, по сравнению с больными I группы — 32±4%.
Нами выработаны следующие противопоказания к эксфузии крови во время операции:
(1) Ht<37%.
(2) ЦВД<5 мм рт.ст.
(3) АДсист<100 мм рт.ст.
(4) Электрическая нестабильность миокарда.
(5) Исходно низкие функциональные резервы миокарда.
(1) Ht<37%.
(2) ЦВД<5 мм рт.ст.
(3) АДсист<100 мм рт.ст.
(4) Электрическая нестабильность миокарда.
(5) Исходно низкие функциональные резервы миокарда.
(3) Управляемый диурез.
Ещё одним моментом, позволяющим создать условия для бескровной хирургии, является управляемый форсированный диурез, который позволяет повысить уровень Ht без использования донорской эритроцитарной массы. С этой целью мы используем небольшие дозы фуросемида (2,5–7,5 мг) в сочетании со 120 мг эуфиллина. Мы считаем, что форсированный диурез показан в перфузионном периоде, когда Ht<25%, а диурез < 3–5 мл/мин и в постперфузионном периоде при Ht<27% и при темпе диуреза менее 3–5 мл/мин.
(4) Гемофильтрация.
Гемофильтрация — это альтернатива форсированному диурезу во время искусственного кровообращения. Если позволяют условия (технические возможности, наличие в оксигенаторе не менее 1000 мл перфузата), мы отдаём предпочтение гемофильтрации. Показания к этой процедуре следующие:
(1) Ht<23%.
(2) Диурез < 3 мл/ч.
(1) Ht<23%.
(2) Диурез < 3 мл/ч.
(5) Использование больших доз трасилола (апротинина, антигозана).
Теоретической предпосылкой его использования является свойство препарата ингибировать протеазы и тем самым угнетать фибринолиз и оказывать протективное действие на активность тромбоцитов.
Во время операции мы использовали трасилол по двум методикам. Согласно I методике суммарная интраоперационная доза составляла 2 млн. ЕИК и распределялась следующим образом: 600 тыс. ЕИК вводили внутривенно болюсно сразу после вводной анестезии, 600 тыс. ЕИК вводили в первичный объём заполнения аппарата искусственного кровообращения и 800 тыс. ЕИК инфузировали в течение всей операции. Такая методика введения трасилола объясняется коротким периодом его полураспада — 23 мин.
Согласно II методике суммарная интраоперационная доза трасилола составляла 6 млн. ЕИК, и вводили её на тех же этапах, только по 2 млн. ЕИК.
Были получены следующие клинические результаты. В группе больных, которым во время операции вводили трасилол в дозе 2 млн. ЕИК (n = 50), объём интраоперационной кровопотери составил 620±14 мл, а у больных, получавших 6 млн. ЕИК трасилола (n = 50), — 524±25 мл; при этом достоверной разницы в объёме кровопотери между группами не отмечалось. Также не было достоверных различий и в отношении частоты переливания донорской крови в этих группах. В I группе эта частота составила 16%, а в группе больных, где доза трасилола составила 6 млн. ЕИК — 18%. Эти данные свидетельствуют о том, что величина интраоперационной кровопотери не зависит от используемой дозы трасилола, поэтому целесообразно ограничиться минимальной дозировкой препарата — 2 млн. ЕИК. В группе больных, где трасилол не использовался, объём кровопотери составил 852±26 мл, а частота использования донорской крови составила 36%, что было достоверно выше этих же показателей в группах пациентов, которым применяли как 6 млн., так и 2 млн. ЕИК трасилола.
Таким образом, предлагаемый протокол анестезиологического обеспечения бескровной хирургии ИБС позволяет в значительной степени снизить объём интраоперационной кровопотери, частоту переливания донорской крови и её компонентов.
Этот тезис подтверждают следующие данные: до реализации протокола объём кровопотери — 852±17 мл, частота инфузии плазмы 100%, тромбоплазмы 100%, эритроцитарной массы 73%; после реализации протокола объём интраоперационной кровопотери составил 581±19 мл, частота инфузии плазмы 83%, тромбоплазмы 12%, эритроцитарной массы 19% (p<0,05).
9. ПУТИ СОХРАНЕНИЯ КРОВИ ПАЦИЕНТА ПРИ ОПЕРАЦИЯХ НА ОТКРЫТОМ СЕРДЦЕ
Б. В. Шабалкин, Н. А. Трекова, А. Г. Кротовский, А. Г. Яворовский, Г. В. Бабалян, Г. А. Рагимов, И. А. Крапивкин.
Научный центр хирургии РАМН, Москва, Россия.
Научный центр хирургии РАМН, Москва, Россия.
В последние годы происходит значительный рост числа операций на открытом сердце. При этих операциях до последнего времени применялось большое количество донорской крови — до 4 л на одного пациента. Несмотря на успешное проведение самой операции, наблюдается большое количество осложнений связанных с гемотрансфузией, так называемый синдром гомологичной крови, а также заражение пациентов через перелитую кровь инфекционными заболеваниями, такими, как ВИЧ-инфекция и вирусный гепатит.
С 1988 г. в РНЦХ РАМН разработана и применяется программа полной сохранности крови пациента на всех этапах лечения. Её применение предусматривает сохранение и заготовку аутокрови как в предоперационном периоде, во время операции, так и в послеоперационном периоде.
Предоперационный период.
До операции у каждого больного, которому планировалось выполнение операции на открытом сердце, осуществляли забор аутокрови или аутоплазмы в количестве 300–600 мл за 2–3 дня до операции. После забора крови её объём компенсировали введением больному растворов кристаллоидов в соотношении 1:2. Вопрос о показаниях и противопоказаниях к эксфузии крови, времени и её объёме решался лечащим врачом и трансфузиологом, исходя из характера заболевания, состояния больного и предполагаемого вида оперативного вмешательства. Таких пациентов, кому забирали кровь до операции, было более 54% от числа оперированных больных в клинике, что позволило собирать до операции в среднем 433±33 мл аутокрови (6 мл/кг веса). Противопоказаниями для забора аутокрови или аутоплазмы считали следующие факторы: вес больного менее 50 кг, нестабильную гемодинамику, нестабильную стенокардию, снижение гемоглобина менее 12,0 г%.
Операционный период.
Весь операционный период проводили на фоне нормоволемической гемодилюции. Для этого до введения гепарина при стабильной гемодинамике и гематокрите выше 38% производили забор дополнительно ещё 200–400 мл аутокрови с параллельным восполнением кровопотери растворами коллоидов и кристаллоидов, в два раза превышающим эксфузию крови. Это было возможно произвести у 92% пациентов в объёме 300±12 мл аутокрови (4 мл/кг веса). Противопоказаниями для интраоперационного забора аутокрови считали снижение уровня гематокрита ниже 38% и нестабильную гемодинамику.
Оптимальное сочетание предоперационного и интраоперационного забора крови снижало потребность в донорской крови во время операции. Сочетание этих методик было применено у 51% пациентов. В среднем на одного пациента ещё до перфузии было заготовлено 698±9 мл аутокрови.
Хирургическая бригада осуществляла тщательный гемостаз, используя современный электрокоагулятор, особенно обращая внимание на обширную раневую поверхность при выделении внутренней грудной артерии, применяли воск для остановки кровотечения из грудины.
Вся кровь до введения гепарина и после введения протамина сульфата собиралась для последующей реинфузии, объём этой крови составил 477±37 мл у 83% пациентов. Использовали две методики сбора крови из операционной раны. Одна предусматривает специальный аппарат, подсоединённый к «грязному» отсосу, в которой собирали кровь. Другая — использование кардиотомного резервуара от аппарата искусственного кровообращения в качестве ёмкости для сбора аутокрови при помощи «коронарного» отсоса. Независимо от методики сбора крови в резервуар добавляли раствор «глюгицир» для предотвращения свёртывания крови. После отмывания крови аутоэритроциты возвращались больному.
Аппарат искусственного кровообращения заполняли без донорской крови. Использовали ультрафильтрационную гемоконцентрацию при снижении гематокрита менее 22%, если при этом объём крови в оксигенаторе был более 1000 мл. Только снижение уровня гематокрита ниже 25% во время искусственного кровообращения являлось показанием для переливания гомологичной крови, что потребовалось у 21% пациентов.
Весь период операции проводилась инфузия апротинина (Trasylol) в дозе 2 млн ЕИК. Введение этой дозы апротинина приводит к ингибированию плазмина и калликреина, а также снижает фибринолитическую активность. Происходит защита тромбоцитов на молекулярном уровне и сохранение их действия в послеоперационном периоде. При применении апротинина наблюдалась почти полная нормализация времени кровотечения после искусственного кровообращения, что свидетельствует о сохранении функции тромбоцитов. Применение апротинина вдвое снизило интра- и послеоперационную кровопотерю, втрое увеличив число больных, которым не требовалось переливание донорской крови.
Во время операции переливание донорской крови осуществляли только при снижении уровня гематокрита ниже 28% после введения протамина сульфата.
Использование предоперационного и интраоперационного забора крови, сбор всей изливающейся крови с последующей её реинфузией, применение нормоволемической гемодилюции, ограничение показаний для инфузии донорской крови, применение апротинина позволили снизить количество переливаемой донорской крови в операционной с 1163±50 мл до 241±32 мл. Тем самым увеличилось количество пациентов без переливания гомологичной крови в операционной до 56%.
Послеоперационный период.
Кровь, изливающаяся по дренажам, стерильна в течение ближайших 8 послеоперационных часов, в этой крови несколько снижен уровень гемоглобина по сравнению с гемоглобином пациента, не содержится фибриноген, и именно поэтому она не сворачивается и к ней не нужно добавлять раствор консерванта при реинфузии.
Во избежание безвозвратной кровопотери в послеоперационном периоде кардиотомный резервуар в операционной подсоединяли к дренажам из полости перикарда и средостения. В отделении реанимации к резервуару подсоединяли вакуум с разрежением 20 см вод.ст. Для реинфузии крови из кардиотомного резервуара к его выходной трубке подсоединяли систему для переливания крови. При кровотечении, с помощью роликового насоса «инфузомата» аутокровь реинфузировали пациенту. Возможен сбор «дренажной» крови из кардиотомного резервуара в специальные мешки для отмывания крови, и уже потом можно аутоэритроциты переливать пациенту. Показанием для реинфузии «дренажной» крови считали кровопотерю с темпом более 100 мл/ч в течение 6–8 послеоперационных часов, подобных наблюдений было 35. Осложнений, связанных с реинфузией «дренажной» крови, не наблюдали.
В ближайшем послеоперационном периоде у 37% пациентов потребовалось переливание донорской крови в количестве 506±75 мл. Показанием для гемотрансфузии в отделении реанимации считали снижение уровня гематокрита ниже 28%.
Общее количество пациентов, кому не переливали донорскую кровь в стационаре составило 36%. Среднее количество использованной донорской крови на одного пациента было 543±50 мл крови, в то время как до принятия программы сохранения крови — 2163±74 мл.
Программа полной сохранности крови пациента имеет медицинский, социальный и экономический эффекты. Количество инфекционных осложнений снизилось в два раза у пациентов без переливания донорской крови. Значительно меньше были затраты на пребывание пациента в стационаре, не говоря уже о предотвращении распространения инфекционных заболеваний.
10. РЕИНФУЗИЯ КАК ИНТРАОПЕРАЦИОННЫЙ МЕТОД СБЕРЕЖЕНИЯ КРОВИ ПАЦИЕНТОВ В СЕРДЕЧНОСОСУДИСТОЙ ХИРУРГИИ
И. А. Крапивкин, А. А. Рагимов, Б. В. Шабалкин, Ю. В. Белов, А. Г. Яворовский, А. Г. Кротовский.
Научный центр хирургии РАМН, Москва, Россия.
Научный центр хирургии РАМН, Москва, Россия.
Актуальность проблемы реинфузии аутокрови как одного из кровосберегающих методов в сердечно-сосудистой хирургии бесспорна. Кровопотеря — постоянный спутник оперативных вмешательств. Сохранить излившуюся кровь, собрав её из операционной раны, вернуть, не подвергая пациента риску возникновения гемотрансфузионных осложнений, вот основные задачи, которые должна решить реинфузия.
Больные теряют кровь не только в операционной, но в послеоперационном периоде. Поэтому реинфузия должна сопровождать пациента от начала операции до первых 8 ч нахождения его в отделении интенсивной терапии или реанимации.
Реконструктивные операции на сердце, коронарных и магистральных артериях, несмотря на постоянное совершенствование хирургической техники, применение современных материалов, сопровождаются кровопотерей, достигающей иногда 10 и более литров.
Как видно из табл. 1, наибольшую величину кровопотери имеют операции на торакоабдоминальном и брюшном отделах аорты (от 2,0 до 10,5 л). Операции аортокоронарного шунтирования, также часто сопровождаются значительной (иногда до 2,5 л) кровопотерей.
Таблица 1. Кровопотеря при операциях на аорте и её ветвях
Характер оперативных вмешательств
|
Число операций
n = 276 |
Объём кровопотери, мл
| ||
Min
|
Max
|
Средний M±m
| ||
На торакоабдоминальном отделе аорты
| ||||
резекция аневризмы и протезирование аорты
|
35
|
7000
|
10500
|
7900±900
|
На брюшном отделе аорты
| ||||
протезирование аорты
|
54
|
3000
|
7500
|
4078±254
|
на ветвях брюшной аорты
|
30
|
2000
|
6500
|
3907±315
|
Реконструктивные операции на сегментах
| ||||
подвздошно-бедренном
|
46
|
600
|
1500
|
1065±340
|
бедренно-тибиальном
|
26
|
200
|
600
|
468±145
|
Аортокоронарное шунтирование
|
85
|
500
|
2500
|
1165±234
|
Компенсация острой кровопотери, в особенности массивной, представляет сложную задачу, а от её качественного выполнения нередко зависит исход оперативного вмешательства.
Любая гемотрансфузия — это вмешательство во внутреннюю среду организма, его гомеостаз, иммунную систему.
При массивной кровопотере, когда больному переливается большое количество консервированной крови разных сроков заготовки от многих доноров, возникает серьёзная опасность развития гемотрансфузионных осложнений, которые встречаются в 5,4% всех переливаний. Гемотерапия должна быть рекомендована лишь тогда, когда она жизненно необходима.
К переливанию крови следует относиться как к операции трансплантации ткани организма со всеми вытекающими из этого последствиями — возможным отторжением клеточных и плазменных компонентов крови донора. У больных с иммунодепрессией переливание донорской крови чревато развитием вторичной болезни — «реакции трансплантата против хозяина».
Экспериментальными и клиническими исследованиями доказано, что использование компонентов донорской крови для возмещения операционной кровопотери не отвечает в полной мере задачам поддержки гомеостаза. В настоящее время следует говорить об особом «гематологическом риске», которому подвергаются оперируемые пациенты.
Переливая собственную кровь больного, можно во многом разрешить проблему компенсации операционной кровопотери, исключить опасность гемотрансфузионных реакций и осложнений, таких, как ошибочное переливание иногруппной или резус-несовместимой крови, перенос инфекционных заболеваний, в том числе гепатита, сифилиса, СПИДа и многих других.
Основными методами сбережения крови являются:
Реинфузия аутокрови — это безопасный метод аутогемотрансфузии, который значительно сокращает объём используемых компонентов донорской крови, а в ряде случаев позволяет вообще обходиться без них.
В самом деле, эта простая по технике выполнения манипуляция спасает жизнь. Удивительно, что многие поколения хирургов осушали операционную рану тампонами, вместо того чтобы собрать эту кровь и вернуть её больному.
Сообщения о применении реинфузии аутокрови начали появляться ещё в XIX веке. В основном её использовали врачи-гинекологи.
В 1925 г. о реинфузии как о методе сообщил основоположник отечественной трансфузиологии А. Н. Филатов. Переливая аутокровь с целью борьбы с операционным шоком, он доказал необходимость фильтрации собираемой крови и важность добавления в неё стабилизирующего раствора.
«Если больной во время операции теряет кровь — ему её обязательно надо вернуть» — таков был принцип хирургов тех лет.
В дальнейшем фундаментальными исследованиями многих отечественных авторов (Б. В. Петровский, Е. А. Вагнер и др.) была доказана высокая эффективность обратного переливания крови — реинфузии.
В 80-х гг. в операционных Научного центра хирургии стала применяться Программа максимального сохранения крови больных и минимального использования компонентов донорской крови.
Важнейшим преимуществом реинфузии аутокрови перед трансфузиями компонентов донорской крови является её быстрое применение — «она практически под рукой у хирурга». Отсутствие реакций несовместимости и исключение возможности переноса инфекционных заболеваний делают её безопасной. Более того, при реинфузии в сосудистое русло возвращается кровь, содержащая иммунные тела, свойственные данному лицу, что способствует повышению иммунной реактивности и сопротивляемости организма пациента инфекции в послеоперационном периоде.
Реинфузия показана практически при всех операциях, требующих гемокоррекции. Это операции, сопровождающиеся массивной кровопотерей, открытые операции на сердце с использованием искусственного кровообращения, операции пациентам с редкими группами крови и затруднёнными гемотрансфузиями пациентам по религиозным соображениям.
Однако, обладая бесспорными преимуществами, метод реинфузии имеет и свои недостатки:
— повреждение форменных элементов крови в момент сбора, что приводит к повышению содержания в ней свободного гемоглобина, то есть к гемолизу;
— опасность бактериального загрязнения во время нахождения вне сосудистого русла;
— трудность сбора крови без сгустков;
— снижение содержания в собранной крови фибриногена и тромбоцитов;
— высокая фибринолитическая и тромбопластическая активность.
Все эти недостатки могут привести к серьёзным, опасным для жизни осложнениям:
Возникновение эмболии связано с образованием в собранной крови сгустков и хлопьев фибрина, закупоривающих мелкие сосуды и капилляры лёгкого. Кроме того, в кровь могут попасть даже отдельные обрывки тканей. Фильтрование реинфузируемой крови через стандартные системы либо через 8 слоёв марли устраняет опасность эмболии.
Переливание инфицированной крови чревато развитием общей гнойной инфекции и может стать причиной смерти больного, поэтому при ранении полых органов, таких, как желудок, кишечник, излившаяся в рану кровь к реинфузии непригодна. Инфицирование крови возможно и во время самого процесса сбора, поэтому реинфузия аутокрови требует строгого соблюдения мер асептики.
Разрушение форменных элементов, в частности эритроцитов, приводит к гемолизу — выходу в плазму свободного гемоглобина. Переливание гемолизированной крови может привести как к гемолитическому шоку, так и к острой почечной недостаточности.
Во всех случаях следует учитывать фактор времени нахождения крови вне сосудистого русла, что связано с вероятностью её внешнего инфицирования.
Морфологический состав аутокрови, собранной во время операции, практически сохранён как в количественном, так и в качественном отношении. Незначительное, не более 25%, снижение числа эритроцитов не обесценивает реинфузируемую кровь, а снижение числа тромбоцитов, связанное с лёгкой ранимостью этих клеток, не переносящих воздействия внешней среды и соприкосновения с окружающими тканями, не вызывает изменений в свёртывающей системе пациентов.
Перелитая аутокровь не депонируется, а сразу же включается в кровоток. Аутоэритроциты циркулируют в сосудистом русле в 1,5–2 раза дольше, чем клетки донорской крови. При оперативных вмешательствах с применением реинфузии, как это можно увидеть в табл. 2, анемии бывают менее выраженными, а восстановление показателей гемоглобина, эритроцитов, гематокрита и ОЦК происходит быстрее, чем переливание компонентов аллогенной крови.
Таблица 2. Зависимость срока нормализации красной крови после операций от величины кровопотери и способа её возмещения (цит. по [10:4])
| Способ возмещения кровопотери | Число больных | Величина кровопотери, мл | Объём возмещения, мл | Срок нормализации красной крови, сут |
|---|---|---|---|---|
Небольшая кровопотеря (до 500 мл)
| ||||
Реинфузия
|
46
|
330,0 ± 12,0
|
275,0 ± 5,7
|
22,8 ± 1,9
|
Донорская кровь
|
22
|
260,0 ± 21,0
|
225,0 ± 6,4
|
32,5 ± 1,5
|
Смешанный
|
38
|
360,0 ± 5,0
|
410,0
|
31,2 ± 1,3
|
Умеренная кровопотеря (510–1000 мл)
| ||||
Реинфузия
|
47
|
745,0 ± 15,0
|
457,0 ± 10,0
|
28,7 ± 0,9
|
Донорская кровь
|
21
|
746,0 ± 30,0
|
960,0 ± 17,0
|
42,5 ± 2,4
|
Смешанный
|
40
|
766,0 ± 25,0
|
810,0 ± 21,0
|
32,3 ± 2,7
|
Массивная кровопотеря (1001–2500 мл)
| ||||
Реинфузия
|
10
|
1280,0 ± 75,0
|
960,0 ± 70,0
|
32,0 ± 3,2
|
Смешанный
|
35
|
1550,0 ± 60,0
|
1730,0 ± 24,0
|
40,4 ± 1,9
|
Это различие объясняется тем, что аутокровь функционирует полноценнее и длительнее, поскольку продолжительность жизни аутоэритроцитов больше донорских. По сравнению с донорской кровью реинфузия аутокрови оказывает более выраженный клинический эффект по выведению больного из тяжёлого состояния.
Динамика восстановления показателей красной крови после малых, средних и больших объёмов возмещения кровопотери донорской кровью либо при сочетании её с реинфузией аутокрови показала, что послеоперационная анемия ликвидируется в начале или в середине второго месяца после операции. При возмещении кровопотери только реинфузией аутокрови анемия исчезает уже к концу первого месяца, то есть на 8–14 дней раньше.
Согласно классификации, предложенной Военно-медицинской академией г. Санкт-Петербурга, реинфузии аутокрови подразделяются на: реинфузии в экстренной и плановой хирургии, а в плановой хирургии — во время операции, в послеоперационном периоде, а также реинфузия «аппаратной» крови, то есть крови, оставшейся в оксигенаторе и магистралях аппарата ИК.
В основе метода реинфузии лежат четыре ключевых принципа:
При операциях с использованием искусственного кровообращения методика проведения реинфузии включает в себя:
В процесс реинфузии дополнительно включается сбор кардиоплегического раствора, когда реинфузор работает как гемоконцентратор, а также сбор «аппаратной» крови. На данных этапах стабилизация крови не проводится из-за наличия в ней гепарина.
До настоящего времени во многих стационарах во время операции для эвакуации крови из раневой полости всё ещё применяют простой метод вычерпывания её черпаком с фильтрацией через 8 слоёв стерильной марли в ёмкости с гемоконсервантом для последующего её переливания.
Новая эра аутогемотрансфузии началась в 70-е гг., после изобретения аппаратов, работавших по принципу аспирации излившейся в рану крови вращающимися насосами, её центрифугирования и отмывания.
Все современные аппараты и устройства для реинфузии крови подразделяются на две основных группы:
— аппараты, работающие с использованием всех четырёх принципов реинфузии (сбор и стабилизация, фильтрация, центрифугирование и отмывание), это так называемый Cell Saver;
— устройства, работающие с использованием только первых двух принципов — стабилизации и фильтрации.
Сбор крови из операционной раны или полости с помощью наконечника оригинальной конструкции, позволяющего подавать гемоконсервант непосредственно в рану, осуществляется регулируемым вакуумом, создаваемым аппаратом. Обычно он поддерживается в пределах 80–120 мм рт.ст. Кровь фильтруется и резервируется в ёмкости, откуда с помощью роликового насоса попадает в колокол для центрифугирования крови. Это позволяет отделить эритроциты от плазмы, содержащей свободный гемоглобин. Отмывание эритроцитов производится физиологическим раствором в том же колоколе центрифуги после его наполнения эритроцитной массой. Объём физиологического раствора составляет 1,0 л на каждые 200–250 мл аутоэритроцитной массы.
Полученная суспензия аутологичных эритроцитов с гематокритом от 50 до 65% роликовым насосом перемещается в специальный пластикатный мешок, откуда может быть сразу же перелита больному.
Пациентам, оперированным в Российском научном центре хирургии РАМН, реинфузия аутокрови проводилась как с помощью аппарата Dideco STAT, так и с помощью резервуара для сбора крови аппарата АРПК-1.
Аппарат АРПК-1 был разработан РНЦХ РАМН совместно с ВНИИМП с учётом достоинств и недостатков приборов и устройств, существовавших на настоящий момент. Аппарат позволяет с минимальной травматизацией форменных элементов собирать в резервуар и фильтровать излившуюся в операционную рану кровь.
В резервуаре для сбора крови предусмотрено сменное устройство для «грубой» фильтрации крови от макросгустков, представляющее собой металлический каркас, обёрнутый марлей в 8 слоёв. В настоящее время разрабатываются сменные одноразовые фильтры-вкладыши, представляющие собой капроновую сетку с ячейкой диаметром около 100–120 мкм.
Аппарат можно отнести ко второй группе устройств, использующих в работе первые два принципа реинфузии — стабилизацию и фильтрацию, однако в нём предусмотрена возможность использования третьего и четвёртого принципов путём перевода реинфузата в пластикатные контейнеры для центрифугирования и отмывания его вне аппарата.
При сравнении отмытых эритроцитов, полученных на аппаратах АРПК-1 и Cell Saver существенных различий выявлено не было.
Следует отметить, что при реинфузии аутокрови с помощью Cell Saver необходимо собрать определённое количество крови для полного заполнения ёмкости колокола центрифуги. В противном случае в отмытых аутоэритроцитах гематокрит будет низким (менее 50%). Это делает применение данных аппаратов оправданным лишь при объёмных операциях, где прогнозируемая кровопотеря требует массивных гемотрансфузий. Использование резервуара АРПК-1 позволяет отмывать любые объёмы крови и возвращать отмытые аутоэритроциты с гематокритом 80–85%.
При реинфузии аутокрови с помощью резервуара аппарата АРПК-1 (табл. 3) удаётся снизить трансфузии донорской эритроцитной массы на 75%, а аппаратом «STAT» — на 85%.
Таблица 3. Восполнение операционной кровопотери при операциях на сердце, коронарных и магистральных артериях
Без реинфузии n = 120
|
С реинфузией n = 156
| ||
АРПК-1 n = 138
|
Cell Saver n = 8
| ||
Кровопотеря, л
|
1050,0 ± 275,0
|
1165,0 ± 254,0
|
4576,0 ± 213,0
|
ТРАНСФУЗИЯ
| |||
Отмытые аутоэритроциты, мл
|
–
|
709,6 ± 101,2
|
3570,5 ± 465,0
|
Донорская эритроцитная масса, мл
|
636,0 ± 152,0
|
275,0 ± 75,0
|
374,0 ± 123,0
|
Донорская плазма, мл
|
760,0 ± 50,0
|
856,0 ± 54,0
|
1050,0 ± 75,0
|
Тромбоконцентрат, доза
|
5 ± 2
|
4 ± 1
|
6 ± 2
|
Кристаллоидные растворы, л
|
1,3 ± 0,15
|
2,2 ± 0,1
|
5,0 ± 0,2
|
Коллоидные растворы, л
|
1,3 ± 0,05
|
2,0 ± 0,2
|
2,4 ± 0,25
|
Применение реинфузии аутокрови во время плановых операций на сердце, коронарных и магистральных артериях сокращает объёмы используемых компонентов донорской крови на 60–80%, а в 20–25% всех оперативных вмешательств позволяет полностью от них отказаться.
Снижение объёмов использования аллогенной крови уменьшает затраты на заготовку и переработку донорской крови, а также на лечение посттрансфузионных осложнений, связанных с её использованием.
Выраженный антианемический и иммуностимулирующий эффект реинфузии аутокрови даёт возможность сократить пребывание больного в стационаре, следовательно, делает её экономически и клинически выгодной.
Подводя итог вышеизложенному, можно заключить, что противопоказанием к реинфузии аутокрови является её бактериальное загрязнение. Реинфузия аутокрови показана практически при всех операциях с кровопотерей более 20% объёма циркулирующей крови. Реинфузируемая аутокровь полноценна и клинически более эффективна. Метод реинфузии прост и в сочетании с другими методами аутогемотрансфузии может и должен быть на вооружении любого хирургического стационара.
ЛИТЕРАТУРА
- [10:1] Аббакумов В. В., Дементьева И. И., Михайлов Ю. Е. и др. Реинфузия аутокрови у кардиохирургических больных в раннем послеоперационном периоде. // Гематология и трансфузиология. — 1991, — №2, — С. 20–22.
- [10:2] Аграненко В. А., Скачилова Н. Н. Гемотрансфузионные реакции и осложнения // М., Медицина, 1986.
- [10:3] Брюсов П. Г. Многокомпонентная трансфузионная программа коррекции операционной кровопотери // Тезисы докладов. 2-й Всесоюзный съезд гематологов и трансфузиологов. — 1985, — Львов. — С. 380.
- [10:4] Брюсов П. Г. Неотложная инфузионно-трансфузионная терапия массивной кровопотери // Гематология и трансфузиология. — 1991, — №2, — С. 8–13.
- [10:5] Вагнер Е. А., Тавровский В. М., Ортенберг Я. А. Реинфузия крови. М., Медицина, 1977.
- [10:6] Дементьева И. И., Савкина М. Э., Чарная М. А. и др. О состоянии гемостаза у больных, оперированных в условиях искусственного кровообращения. // Анестезиология и реаниматология. — 1990, — №5, — С. 16.
- [10:7] Инструкция по заготовке эритроцитной массы, обеднённой лейкоцитами и тромбоцитами // МЗ СССР, — М. — 1987, — 18 с.
- [10:8] Крапивкин И. А. Аутогемотрансфузия в хирургии аорты и её ветвей // Дисс. к.м.н., М., — 1997.
- [10:9] Кузминок Б. И., Васильев Н. В., Цыбиков Н. Н. Иммуногенез, гемостаз и неспецифическая резистентность организма. М., 1989.
- [10:10] Лычёв В. Г. Диагностика и лечение диссеминированного внутрисосудистого свёртывания крови. — М. — Медицина. — 1983, С. 159.
- [10:11] Практическая трансфузиология (ред. Козинец Г. И. и др.) М., — 1997, — С. 241–255.
- [10:12] Раби К. Локализованная и рассеянная внутрисосудистая коагуляция: Пер. с франц. — М., 1974.
- [10:13] Руководство по общей и клинической трансфузиологии. Под ред. Б. В. Петровского, М., 1979, С. 236–254.
- [10:14] Сумбатов Л. А., Юновидова Л. И. Проблема гомологичной крови в трансфузиологии и её решение // Гематология и трансфузиология, 1989, — №10, — С. 12–14.
- [10:15] Уманский М. А., Страпко Н. П. Применение метода гемодилюции при операциях на органах брюшной полости. Методические рекомендации. // Киев, 1977, 14 с.
- [10:16] Bretton P., Reines H. D., Sade R. M., // J. Trauma. — 1985. — Vol. 25. — P. 165.
- [10:17] Fisher J. B., Dennis R. C., Valeri C. R. et al. Effect of graft material on loss of erythrocytes after aortic operations. // Surg. Gynecol. Obstet., 1991, — Aug. — V. 173(2), — P. 131–136.
- [10:18] Georgiev G., Rankov S. Autotransfusion in cardio-vasculation surgery. // 1-st Meditarraneon congress of angiology, Abstracts Book, 1988, — P. 110.
- [10:19] Lisander B., Jonsson R., Nordwall A. Combination of blood saving methods decreases homologous blood requirements in scoliosis surgery. // Anaesth Intens Care 1996; 24; 555-8.
- [10:20] Mercurial F. and Inghilleri G. Algorithm to be applied to transfusion practice // НРЖ Трансфузиология, 1988, №1Б, С. 6–7.
- [10:21] Miller A. G. Case of amputation at hip-joint in which reinjection of blood was performed and rapid recovery took place. // Edinburg Med. J., 1985. — V. 31. — P. 721.
- [10:22] Zuck T. F., Patticia M. C. Autologous Transfusion practice controversies about curzent fashion and read needs // Vox. Saung. 1990, — V. 58, — №3, P. 234–253.
11. ПРИНЦИПЫ ЗАМЕСТИТЕЛЬНОЙ ТЕРАПИИ ТРОМБОЦИТОПЕНИЧЕСКОГО СИНДРОМА ПРИ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ У ГЕМАТОЛОГИЧЕСКИХ БОЛЬНЫХ
В. Ю. Баранович, Г. И. Алексеев, В. В. Рыжко, Г. Ю. Белинин, Н. Н. Максимов, Г. И. Веретник, А. С. Кириленко.
Российский университет дружбы народов, ЦКБ им. Н. А. Семашко МПС России.
Российский университет дружбы народов, ЦКБ им. Н. А. Семашко МПС России.
Тромбоциты играют существенную роль в обеспечении сосудисто-тромбоцитарного гемостаза (первичного гемостаза), который реализуется в микрососудах диаметром до 100 мкм. Участие тромбоцитов в гемостазе определяется по крайней мере следующими функциями:
— способностью поддерживать нормальную структуру и функцию стенок микрососудов;
— способностью образовывать в повреждённых сосудах первичную тромбоцитарную пробку за счёт адгезивно-агрегационных свойств;
— способностью поддерживать спазм повреждённых сосудов;
— участие в коагуляционном гемостазе.
Тромбоцитопеническим синдромом считается ситуация, когда число тромбоцитов снижается до 100 000/мкл и ниже.
Клинически проявляется петехиальными высыпаниями и геморрагиями, в первую очередь на коже нижних конечностей, затем на верхней половине туловища, на коже лица, спонтанной кровоточивостью из слизистых рта и носа, кровоизлияниями в конъюнктиву и глазное дно, а также локальными кровотечениями (ЖКТ, матка, почки, мочевой пузырь).
Следовательно, недооценка геморрагического синдрома, обусловленного недостаточным количеством тромбоцитов или нарушением их функциональной способности, в конечном счёте приводит к кровоизлияниям в головной мозг и (или) лёгкие, что обычно заканчивается летальным исходом уже независимо от предпринимаемых мер.
Причины возникновения тромбоцитопенического синдрома (или кровоточивости, обусловленной тромбоцитами):
(а) недостаточное образование тромбоцитов в костном мозге — амегакариоцитарная тромбоцитопения, она возникает у больных с опухолями системы крови и поражением костного мозга (острый лейкоз; хронический лейкоз; саркома), эпителиальные опухоли с метастатическим поражением костного мозга; депрессия костномозгового кроветворения в результате цитостатической терапии, лучевой терапии, трансплантации костного мозга, апластическая анемия и острая лучевая болезнь;
(б) повышение потребления тромбоцитов — ДВС-синдром в фазе гипокоагуляции, ИК, где имеет место не только снижение количества тромбоцитов ниже критического уровня, но и снижение их функциональной активности. (При ДВС-синдроме тромбоциты уже были в сгустках, при ИК имели воздействие чужеродной среды.)
(в) качественная неполноценность тромбоцитов (так называемые тромбоцитопатии) — непостоянная, умеренная тромбоцитопения, обусловленная укорочением продолжительности жизни дефектных тромбоцитов. Это возникает при уремии, при иммунных (тромбоцитолитических) тромбоцитопениях, при тромбоцитопенической пурпуре (болезнь Мошковича).
Если больным с недостаточным образованием тромбоцитов требуется заместительное переливание концентрата тромбоцитов (КТ), то другим — лишь в ургентных случаях. Переливание тромбоцитов с профилактической целью нецелесообразно из-за возможной аллоиммунизации или лизиса донорских тромбоцитов.
Таким образом, конкретные показания для переливания тромбоцитов устанавливаются врачом в зависимости от динамики клинической картины, анализа причин тромбоцитопении и её выраженности.
Каковы же, собственно, принципы заместительной терапии, то есть кому, сколько и когда переливать концентрат тромбоцитов.
17 В неосложнённых случаях снижение числа тромбоцитов до 100 000/мкл само по себе ещё не является катастрофой для функционального состояния организма, хотя при ряде оперативных вмешательств, в частности в нейрохирургии, может привести к осложнениям, поэтому хирург должен ставить вопрос о переливании тромбомассы.
При полостных операциях этого количества тромбоцитов вполне достаточно, если нет нарушения функции тромбоцитов.
Существует простой метод, указывающий на функциональную состоятельность тромбоцитов, — это длительность кровотечения. Если длительность кровотечения увеличивается более чем в два раза, то хирург вправе думать о том, что функция тромбоцитов снижена, и должен опасаться возникновения кровотечения в ходе операции. В случаях, когда количество тромбоцитов снижено до 50 000/мкл, но при этом функция тромбоцитов нормальная, мы можем без переливания КТ идти на мелкие хирургические вмешательства — постановка катетера, биопсия лимфоузла, вскрытие флегмоны.
Но если число тромбоцитов снижается до 20 000/мкл и ниже, то хирург всегда должен идти на операцию, имея тромбоконцентрат, независимо от того, имеются ли клинические проявления тромбоцитопении или их нет (в частности, петехиальные высыпания на коже, кровоточивость носа, дёсен и др.).
В хирургической клинике, связанной с гематологией, есть ряд заболеваний, при которых можно обойтись без инфузии тромбоцитов, это аутоиммунная тромбоцитопеническая пурпура, или болезнь Верльгофа. В этой ситуации подъём уровня тромбоцитов может осуществляться не за счёт трансфузии донорских клеток, а за счёт лекарственных препаратов, таких, как преднизолон или другие стероиды, использование донорских в/в гаммаглобулинов, которые позволяют на короткий период времени поднять уровень тромбоцитов выше критического. И тогда у определённой категории больных сразу после операции или в ходе операции — удаление селезёнки, если эта операция эффективна, — число тромбоцитов нормализуется достаточно быстро.
Необходимым количеством переливаемых тромбоцитов является лечебная доза концентрата тромбоцитов, стандартная доза должна содержать 4–5 × 1011 тромбоцитов. Однако, для каждого конкретного больного количество тромбоцитов может быть подобрано индивидуально. Существуют специальные формулы расчёта требуемого количества переливаемых тромбоцитов для обеспечения гемостатического эффекта:
— 1 × 109 по количеству тромбоцитов в 1 л объёма циркулирующей крови;
— 0,5–0,7 × 109 по количеству тромбоцитов в пересчёте на 10 кг массы тела;
— 2,5 × 109 по количеству тромбоцитов на 1 м2 поверхности тела.
Принципиального различия по результату они не имеют, наиболее практичным и самым распространённым является подсчёт по массе тела больного.
Например, для реципиента с массой тела 70 кг требуемое количество тромбоцитов от 3,5 до 4,9 × 109, оно является достаточным, если состояние реципиента не сопровождается:
— спленомегалией;
— инфекционными осложнениями с гипертермией, сепсисом;
— ДВС-синдромом;
— массивным кровотечением из желудочно-кишечного тракта.
— спленомегалией;
— инфекционными осложнениями с гипертермией, сепсисом;
— ДВС-синдромом;
— массивным кровотечением из желудочно-кишечного тракта.
В этих ситуациях потребность больного в количестве донорских тромбоцитов возрастает на 60–70%. Если в норме секвестрация в селезёнке 1/3, то при спленомегалии может достигать 80–90%. Это необходимо учитывать, особенно в преддверии хирургических операций. То же самое у больных с ДВС-синдромом и перенёсших ИК, у которых число тромбоцитов может быть даже выше критического уровня, но его тромбоциты функционально не полноценны.
В этих случаях в клинической практике хирурга опять может помочь определение длительности кровотечения (не свёртываемость крови, а именно длительность кровотечения), и при её увеличении в два раза в ходе операций или после них во избежание послеоперационных кровотечений, конечно, необходимо использование тромбоконцентрата.
Наиболее эффективно действие тромбоконцентрата, перелитого в течение первых 24 ч с момента его получения. Во избежание аллоиммунизации используют ТК от доноров-родственников (при необходимости забор крови можно у них осуществлять до трёх раз в неделю).
Клиническими критериями эффективности трансфузий тромбоцитов являются: прекращение спонтанной кровоточивости и отсутствие свежих геморрагий на коже и видимых слизистых.
Лабораторными признаками являются: увеличение количества тромбоцитов у реципиента через час после трансфузии (не менее 5–6 × 1011/л) и их повышенное содержание через 24 ч; коррекция длительности кровотечения у больного через час и через 24 ч после трансфузии.
Оптимальному режиму трансфузии, при котором нормализуется длительность кровотечения, обычно соответствует концентрация тромбоцитов в периферической крови 40 000/мкл и выше.
Осложнения трансфузии тромбоцитов зависят от: метода их получения, правильного обследования и выбора донора, соблюдения условий хранения и наличия в КТ других форменных элементов крови.
Осложнениями являются:
— аллоиммунизация — сенсибилизация реципиента — характеризуется появлением антитромбоцитарных антител. Проявляется температурной реакцией, отсутствием должного прироста тромбоцитов и гемостатического эффекта. Основной причиной является загрязнение КТ лейкоцитами. Во избежание данного явления предпочтительны доноры-родственники или доноры костного мозга. В качестве лечебной процедуры используют плазмаферез, позволяющий удалить из циркуляции аллоантитела;
— анафилактический шок — источником считаются протеины донорской плазмы — это реакция гиперчувствительности немедленного типа. Антигистаминные препараты или премедикация позволяют осуществить трансфузию без серьёзных последствий;
— реакция «трансплантат против хозяина» возникает у больных с тяжёлым комбинированным иммунодефицитом, наиболее высок риск при пересадке костного мозга у детей с синдромом тотального иммунодефицита, с Т-клеточным иммунодефицитом и больных хроническим лимфолейкозом. Можно предупредить, облучая ТК перед трансфузией в дозе 1500–5000 рад.
Инфекционные осложнения:
— посттрансфузионный бактериальный эндотоксический шок; посттрансфузионный гепатит (2–5% реципиентов, из них у 10–20% развивается цирроз или рак печени);
— СПИД — погрешности в исследованиях или «диагностическое окно»;
— цитомегаловирусная инфекция;
— другие вирусы — мононуклеоз, парвовирус;
— паразитарные инфекции — малярия, токсоплазмоз, сифилис, филяриоз, бруцеллёз.
Также возможна передача других, ещё не открытых и не тестируемых агентов.
Несмотря на сложность приготовления, непродолжительные сроки хранения и возможные грозные осложнения, трансфузия тромбоцитов является важнейшей лечебной процедурой, позволяющей подготовить больного к операции, выполнить оперативное вмешательство и провести послеоперационный период.
Нозология
|
Предоперационная подготовка
|
Операция
|
После операции
| |||
% больных
|
Кол-во доз КТ
|
% больных
|
Кол-во доз КТ
|
% больных
|
Кол-во доз КТ
| |
Апластическая анемия
|
100
|
2–6
|
100
|
2–4
|
100
|
2–4
|
Лимфоцитома селезёнки
|
30–50
|
1–4
|
30–50
|
1–2
|
10
|
1–2
|
Волосатоклеточный лейкоз
|
80–100
|
2–4
|
80–100
|
2–3
|
50
|
1–2
|
Хронический миелолейкоз
|
80–100
|
2–6
|
50–100
|
2–6
|
40–60
|
1–4
|
Аутоиммунная тромбоцитопения
|
–
|
–
|
–
|
–
|
–
|
–
|
12. ИНТРАОПЕРАЦИОННЫЙ АУТОЗАБОР КРОВИ КАК СПОСОБ ЕЁ СОХРАНЕНИЯ ПРИ ОПЕРАЦИЯХ У ОРТОПЕДИЧЕСКИХ БОЛЬНЫХ
С. В. Сергеев, М. А. Абдулхабиров, А. В. Джоджуа, Л. И. Зелёнкина.
ГКБ №20, Кафедра травматологии и ортопедии Российского университета дружбы народов, Москва, Россия.
ГКБ №20, Кафедра травматологии и ортопедии Российского университета дружбы народов, Москва, Россия.
Прогноз послеоперационного выздоровления травматологических больных во многом зависит от операционной кровопотери и от грамотной инфузионно-трансфузионной терапии для её возмещения.
Травма, сопровождающаяся множественными переломами и переломами длинных трубчатых костей, костей таза, приводит к выраженным изменениям объёма циркулирующей крови, состояния гемодинамики и состава периферической крови, а также является пусковым механизмом коагулопатии. Таким образом, тактика инфузионно-трансфузионной терапии и замещения операционной кровопотери должна учитывать указанные выше обстоятельства. Известно несколько методов возмещения операционной кровопотери: переливание донорской крови, аутокрови, реинфузия излившейся крови во время операции.
В последние годы оценка возмещения операционной кровопотери донорской кровью существенным образом изменилась. Наряду с гемотрансфузионными реакциями были выявлены и посттрансфузионные осложнения. При этом частота их возникновения существенно возрастала в зависимости от числа доноров и увеличения дозы переливаемой крови. Риск, связанный с гемотрансфузией, может превысить её лечебный эффект.
По свидетельству многих авторов, большие гемотрансфузионные конфликты не так уж редки, наблюдаются в 0,003% всех переливаний крови и заканчиваются, как правило, летально (Головин Г. В. и др., 1975 г.). Вероятно, не менее часты несовместимые переливания крови по антигенам эритроцитов не только системы ABO, но и систем Келл, P, Лютеран, Донн-Брокк, которые также тяжело протекают, но ещё недостаточно распознаются.
Можно предположить, что ещё долгое время подбор крови донора и реципиента по антигенам лейкоцитов, тромбоцитов, плазменных систем останется невозможным. Также могут наблюдаться посттрансфузионные реакции аллергического типа, частота которых доходит до 12% (Беленький Д. Н., Аграненко В. А. и др., 1979 г.).
В принципе каждое введение в организм донорской крови является не чем иным, как операцией пересадки органа или ткани, со всеми иммунологическими проблемами подбора и совместимости. Немало инфекционных осложнений, связанных с переливанием донорской крови, прежде всего заражение реципиента сывороточным гепатитом, ВИЧ-инфекцией. Кроме того, независимо от сроков хранения до 30% консервированных эритроцитов находятся в крови в виде агрегатов, которые при переливании оседают в лёгких (Альес В. Ф., Андреев А. Г., Астамиров М. К.). Это приводит к увеличению «мёртвого пространства» и усилению лёгочного шунтирования. До 25–30% перелитых донорских эритроцитов депонируются в органах и тканях (Афонин и др.). Следует помнить и об экономической стороне этой проблемы.
Учитывая возможные осложнения при переливании донорской крови, в последние годы большой интерес вызвала методика возмещения операционной кровопотери аутокровью (заранее заготовленная, полученная из раны при оперативном вмешательстве, «дренажная» кровь). Различными авторами доказано, что при возмещении операционной кровопотери аутокровью не происходит её депонирования и одна доза собственной крови может заменить 2–4 дозы донорской крови, а продолжительность жизни аутоэритроцитов в 1,5–2 раза превышает продолжительность жизни донорских эритроцитов (Козинец Г. И. и др., 1996 г., Афонин и др., 1998 г.).
Применение методик аутогемотрансфузии и реинфузии крови позволило значительно сократить потребность в донорской крови для возмещения операционной кровопотери. Возможна предоперационная заготовка аутокрови за несколько дней до операции с целью возмещения операционной кровопотери. Альтернативой этой методике является интраоперационный аутозабор крови, который представляет собой технику заготовления собственной крови непосредственно перед операцией и намного дешевле плановой заготовки аутокрови (Terri G. Monk, Lawrence T. Goodnough и др., 1998 г.). Однако ценность интраоперационной заготовки крови спорна, и в отличие от планового аутозабора этот способ находится в стадии разработки. ИЗК — самый дешёвый метод сохранения крови. Во-первых, единицу собственной крови, полученную с помощью ИЗК, переливают обратно пациенту ещё в операционной — не требуется расходов на инвентарь и на тестирование крови. Этот метод также исключает возможность административной ошибки, которая может привести к переливанию ABO-несовместимой крови и смерти. Во-вторых, так как заготовка крови с помощью ИЗК и реинфузия производится прямо в операционной и персоналом, находящимся в ней, то расходы сводятся до минимума. Кроме того, установлено, что оптимальным сроком для проведения оперативного вмешательства после эксфузии крови при плановом аутозаборе является 3–4 сут. Но за это время происходят изменения состава крови (Козинец Г. И. и др., 1997 г.). Лейкоциты погибают за первые сутки, тромбоциты за 48 ч. В эритроцитах во время хранения крови продолжают происходить процессы обмена веществ, что ведёт к накоплению молочной кислоты с «закислением» крови. Основная функция эритроцитов — перенос кислорода — прогрессивно падает уже в первые дни хранения крови, клетки красной крови быстро теряют АТФ, необходимый для связывания кислорода гемоглобином.
В связи с вышеизложенным мы хотели бы доказать, что ИЗК является безопасным, эффективным и недорогим методом замещения операционной кровопотери. Кроме того, травматические ортопедические операции сами по себе являются дорогостоящими, в связи с чем данный метод замещения операционной кровопотери заслуживает внимания.
Целью нашей работы является выработка тактики адекватного возмещения операционной кровопотери собственной кровью пациента с минимальными затратами и максимальной эффективностью. Для достижения этой цели мы поставили следующие задачи:
(1) Разработать показания и противопоказания для предоперационного планового аутозабора и интраоперационного аутозабора.
(2) Дать оценку изменениям объёма циркулирующей крови, показателям гемодинамики и гомеостаза.
(3) Проанализировать количество и характер послеоперационных осложнений в зависимости от степени операционной кровопотери и метода её возмещения с применением аутокрови.
Для сравнительного анализа мы разбили больных на 3 группы:
(1) Больные, которым во время операции была перелита донорская кровь.
(2) Больные, которым был сделан плановый аутозабор крови.
(3) Больные с интраоперационным аутозабором крови.
(1) Больные, которым во время операции была перелита донорская кровь.
(2) Больные, которым был сделан плановый аутозабор крови.
(3) Больные с интраоперационным аутозабором крови.
Суть метода интраоперационного аутогемозабора заключается в эксфузии части крови больного непосредственно перед началом хирургического вмешательства и восполнении потерянного объёма крови плазмозамещающими растворами, что обеспечивает стабильность гемодинамики. Для компенсации потери объёма циркулирующей крови при интраоперационном аутогемозаборе используют как растворы кристаллоидов (раствор Рингера с лактатом), так и растворы коллоидов (альбумин, декстраны, гидроксиэтилкрахмал, желатиноль). Однако эффективность этих препаратов различная. В случае применения кристаллоидов приходится вводить тройное количество раствора сравнительно с отобранным объёмом крови. Кроме того, при длительном хирургическом вмешательстве, когда необходимо дополнительное вливание жидкости, она скапливается в интерстициальном пространстве и образует выраженные отёки. Преимущество кристаллоидов заключается в быстроте их действия. В связи с перечисленными причинами гемодилюцию кристаллоидами мы производим в случае кратковременного хирургического вмешательства и небольшой операционной кровопотери, в среднем 500 мл. При длительном хирургическом вмешательстве и значительной кровопотере до 1000 мл гемодилюция производится, дополнительно к кристаллоидам, коллоидными растворами объёмом в среднем 800 мл.
Расчёт допустимого объёма забора крови проводится индивидуально, учитывая возраст, пол, общее состояние пациента, показатели гомеостаза, Hb, Ht, ожидаемую кровопотерю. Эксфузия крови выполняется при стабильной гемодинамике. Критерии интраоперационного, а также планового аутогемозабора: больные не старше 70 лет, гемоглобин не ниже 110 г/л, гематокрит не ниже 30%. Также противопоказанием являются тяжёлые сопутствующие соматические заболевания, при которых снижены компенсаторные способности сердечно-сосудистой системы. Интраоперационный аутогемозабор проводят больным с ожидаемой кровопотерей от 400 до 1000 мл. В среднем мы забираем от 300 до 500 мл крови. Эксфузия крови происходит в пластиковый мешок с гемоконсервантом, который хранится при комнатной температуре. В то же время проводят немедленное замещение крови кристаллоидными растворами в соотношении 1:3 соответственно (гиперволемическая гемодилюция). В последующем отобранная кровь переливается больному по мере кровопотери, обусловленной хирургическим вмешательством. При интраоперационном аутогемозаборе теряемая больным кровь содержит сниженное количество эритроцитов. Несмотря на то что проведение гиперволемической гемодилюции сопровождается снижением гематокрита до 20–25%, риск развития гипоксии у больных не увеличивается. Напротив, улучшается кровоток и оксигенация тканей за счёт уменьшения общего периферического сопротивления и повышения ударного индекса и сердечного выброса (Альес В. Ф., Андреев А. Г., Астамиров М. К., 1997 г.).
Нами проанализированы данные динамики восстановления гомеостаза 17 больных, которым был произведён аутогемозабор (9 из них с интраоперационным аутогемозабором и 8 — с плановым), а также 12 больных, при оперировании которых была использована донорская кровь. Все операции сделаны на проксимальном и диафизарном отделе бедра. По нашим наблюдениям, при изначальном показателе гемоглобина 130–140 г/л и гематокрита 35–40% в вышеперечисленных трёх группах больных происходит различное снижение показателей гемоглобина и гематокрита в послеоперационном периоде, а также их восстановление.
При интраоперационном аутогемозаборе предельное снижение показателей гемоглобина и гематокрита происходит к первой неделе после операции (до Hb 95–100 г/л, Ht 30–35%) и полное восстановление до исходных цифр — к концу второй недели.
При плановом аутогемозаборе максимальное снижение гемоглобина до 90–95 г/л и гематокрита до 30–35% происходит уже к третьему дню после операции и держится на низком уровне до двух недель. Полное восстановление в среднем происходит к третьей неделе. В обеих группах не отмечалось ни одного случая посттрансфузионных осложнений.
При использовании донорской крови минимальные показатели гемоглобина до 80–85 г/л и гематокрита до 20–25% наблюдаются в первые две недели после операции, к третьей неделе отмечается тенденция к нормализации гемоглобина и гематокрита. Восстановление до изначальных показателей гомеостаза в среднем отмечается к четырём неделям. Кроме того, в третьей группе пациентов наблюдались различного рода посттрансфузионные осложнения: у двух больных отмечалась аллергическая реакция на трансфузию донорской крови, в одном случае наблюдалась посттромбоэмболическая пневмония.
Метод аутогемотрансфузии является простым и доступным в любом стационаре, позволяет предотвратить ряд тяжёлых осложнений, которые отмечаются при трансфузии донорской крови, уменьшить потребность в переливании донорской крови.
Таким образом, очевидно превосходство метода замещения операционной кровопотери аутокровью. С целью более детального изучения этого вопроса в нашей клинике продолжается работа в данном направлении.
Номограмма восстановления Hb в крови у послеоперационных больных
|
Ряд
|
■
|
— больные с интраоперационным аутогемозабором.
|
Ряд
|
▲
|
— больные с плановым аутогемозабором.
|
Ряд
|
✖
|
— больные, которым переливалась донорская кровь.
|
13. ПРИМЕНЕНИЕ АУТОТРАНСФУЗИЙ В УСЛОВИЯХ МНОГОПРОФИЛЬНОЙ БОЛЬНИЦЫ
Г. Ю. Белинин, В. В. Рыжко, С. А. Васильев, В. Ю. Баранович, Г. И. Алексеев, А. С. Кириленко, Г. И. Веретник, В. И. Гунько.
ЦКБ МПС им. Н. А. Семашко, Кафедра гематологии и интенсивной терапии РМАПО, Кафедра госпитальной хирургии Российского университета дружбы народов, Москва, Россия.
ЦКБ МПС им. Н. А. Семашко, Кафедра гематологии и интенсивной терапии РМАПО, Кафедра госпитальной хирургии Российского университета дружбы народов, Москва, Россия.
Аутотрансфузионная терапия в ЦКБ МПС им. Н. А. Семашко проводится по трём основным направлениям.
(1) Плановая заготовка аутокомпонентов крови у больных перед оперативными вмешательствами.
(2) Проведение аутотрансплантации стволовых клеток крови при гемобластозах.
(3) Проведение селективного плазмафереза у больных с иммунокомплексной патологией с использованием очищенной аутоплазмы для плазмозамещения.
Плановая заготовка аутоэритроцитной массы и аутоплазмы производится за 4–10 дней до предполагаемого оперативного вмешательства при ожидаемой операционной кровопотере более 500 мл. В сдвоенный пластиковый контейнер для заготовки крови с консервантом CPDA-1 набирается, в среднем, 500 мл цельной крови больного, которая затем центрифугируется и разделяется на эритроцитную массу и плазму. Возмещение объёма производится растворами кристаллоидов. Плазма сразу же после отделения замораживается и хранится при −30°C; эритромасса хранится при +4°C не более 14 дней. Аутогемотрансфузии проводятся по показаниям во время операций и/или в раннем послеоперационном периоде.
В период 1994–1998 гг. в больнице произведена плановая заготовка аутокомпонентов крови у 50 больных: 22 женщин и 28 мужчин в возрасте от 16 до 59 лет. Распределение больных по годам и клиническим отделениям представлено в таблице.
Клинические отделения
|
По годам
|
Всего
| ||||
1994
|
1995
|
1996
|
1997
|
1998
| ||
Травматология
|
2
|
1
|
1
|
2
|
2
|
8
|
Нейрохирургия
|
2
|
7
|
6
|
7
|
2
|
24
|
Челюстно-лицевая хирургия
|
–
|
–
|
–
|
6
|
10
|
16
|
Общая хирургия
|
–
|
1
|
1
|
–
|
–
|
2
|
Всего
|
4
|
9
|
8
|
15
|
14
|
50
|
Показаниями к плановой заготовке аутокомпонентов крови у больных перед оперативными вмешательствами являлись:
— нормальный уровень гемоглобина и количества эритроцитов в крови;
— нормальное или повышенное артериальное давление;
— отсутствие выраженной патологии со стороны органов и систем, септических симптомов;
— отсутствие декомпенсации по основному заболеванию.
Контрольные уровни гемоглобина и эритроцитов у больных после эксфузии крови оставались в пределах нормы; осложнений во время эксфузий и аутогемотрансфузий не было.
Следующим направлением проведения аутогемотрансфузионной терапии в ЦКБ МПС им. Н. А. Семашко является разработанная и впервые в 1988 г. в России осуществлённая аутотрансплантация стволовых клеток крови (СКК) при гемобластозах. Всего проведено 17 аутотрансплантаций СКК: 10 больным острым нелимфобластным лейкозом (3 — резистентность, 6 — рецидивы, 1 — первая ремиссия); 5 больным множественной миеломой (4 — резистентность, 1 — рецидив) и 2 больным лимфогранулематозом (1 — резистентность, 1 — рецидив). Возраст больных от 13 до 49 лет.
Получение СКК осуществлялось на сепараторе клеток крови CS-3000 («Baxter», США) во время выхода больных из миелотоксического агранулоцитоза после проведения курса химиотерапии. Количество процедур лейкоцитафереза составляло от 3 до 8; за одну процедуру перерабатывалось 10 л крови больного, объём лейкоконцентрата составлял 0,2 л; полученный лейкоконцентрат хранили в банке костного мозга ОНЦ РФ. Кроме того, в процессе лейкоцитафереза осуществлялась заготовка 1–2 л аутоплазмы для применения в посттрансплантационный период.
Заготовка аутотромбоцитной массы не проводилась из-за короткого срока хранения (при комнатной температуре в тромбомиксере не более 5 дней); при хранении тромбоцитов в жидком азоте жизнеспособными остаются только 30%. Кондиционирование у больных острыми лейкозами проводилось по программе BACT, у больных множественной миеломой — алкеран + циклофосфан, у больных лимфогранулематозом — CBV. После проведения аутотрансплантации восстановление лейкоцитов до 1000/мкл и тромбоцитов до 50 000/мкл происходило на +20 (+8…+35) и +27 (+9…+54) дни.
В 1987 г. нами была начата разработка методик проведения селективного плазмафереза, заключающегося в том, что удаляемая в процессе проведения плазмафереза аутоплазма больного не выбрасывается, а очищается и применяется для возмещения удалённого объёма во время следующих операций плазмафереза. Первым разработанным нами методом очищения плазмы крови больных был метод гепаринокриопреципитации, в основе которого лежит способность плазменного белка фибронектина в присутствии гепарина связывать и выводить из циркуляции патологические белковые комплексы.
В результате дальнейших поисков более эффективных методов очищения плазмы крови нами был разработан и предложен для клинического применения метод гепаринокриофракционирования плазменных белков, заключающийся в добавлении в отделённую при плазмаферезе плазму больного гепарина, замораживании её и центрифугировании в замороженном состоянии при +21–+22°C со скоростью 3500 об/мин в течение 40–45 мин. Супернатант отделяется от осадка, и очищенная аутоплазма применяется для плазмозамещения в процессе проведения следующей операции плазмафереза. Из плазмы крови больных элиминируются следующие компоненты: в среднем, 84% фибронектина, 38% фибриногена, 92% фактора Виллебранда, 8% альбумина, 8% IgG, 5% IgM, 95% комплексов фибронектин-фибрин, 93% комплексов фибронектин-C1q-субкомпонент комплемента, 90% комплексов фибронектин-IgG, 100% криоглобулинов I, II, III типов и криофибриноген.
Этот способ селективного плазмафереза был применён в лечении 82 больных (23 мужчин и 59 женщин в возрасте от 15 до 75 лет) с иммунокомплексной патологией, которым, в целом, было проведено 415 операций. 35 больных страдали ревматоидным артритом, 19 — геморрагическими васкулитами, 15 — системной красной волчанкой, 4 — болезнью Бехтерева, 3 — синдромом Шегрена, 3 — хроническим вялотекущим увеитом, 2 — иммунокомплексным синдромом, 1 — системной склеродермией. За одну операцию удалялось, в среднем, 1,5 л плазмы; объём очищенной аутоплазмы, используемой для плазмозамещения, составил, в среднем, 1,3 л (86%).
Полный курс лечебного селективного плазмафереза состоял из 4–6 операций в течение 1,5–2 нед. Положительный клинико-лабораторный эффект был получен у всех больных: наблюдалась регрессия клинических симптомов заболевания, вплоть до полного их исчезновения; было выявлено значительное возрастание микроциркуляторного кровотока по данным бульбарной микроскопии и капилляроскопии ногтевого ложа; значительно снизились лабораторные показатели активности заболевания. При этом уровни общего белка крови, альбумина, нормальных иммуноглобулинов и плазменного фибронектина достоверно не изменились и оставались в пределах нормы. Динамическое наблюдение за больными в течение 6–12 мес показало устойчивость полученного клинико-лабораторного эффекта. Повторного проведения курса лечения за этот период не потребовалось.
Применяемая в отделении гравитационной хирургии крови ЦКБ МПС им. Н. А. Семашко методика селективного плазмафереза с очищением плазмы крови больного методом гепаринокриофракционирования и использованием очищенной аутоплазмы для плазмозамещения является высокоэффективным способом лечения больных с наличием гиперкоагуляционного синдрома, системного васкулита различной этиологии, нарушений микроциркуляции, местных воспалительных процессов с развитием фиброзирующих изменений в местах тканевого и сосудистого повреждения при заболеваниях иммунокомплексного генеза.
Данная методика позволяет полностью отказаться от применения для плазмозамещения компонентов и препаратов донорской крови, что устраняет риск инфекционных (гепатиты, ВИЧ-инфекция и пр.) и аллергических осложнений у больных, а также значительно снижает материальные затраты на проведение операций плазмафереза и уменьшает сроки лечения больных и частоту рецидивов.
14. ПРИМЕНЕНИЕ АУТОГЕМОТРАНСФУЗИИ В УСЛОВИЯХ МНОГОПРОФИЛЬНОЙ БОЛЬНИЦЫ
М. М. Петров, Г. К. Орлова, В. М. Городецкий, А. И. Воробьёв, С. В. Варламова, Е. А. Мовсесьян.
ГНЦ РАМН, Москва, Россия.
ГНЦ РАМН, Москва, Россия.
В настоящее время в клинической трансфузиологии всё возрастающее значение отводится аутогемотрансфузии. Преимущества аутологичных трансфузий компонентов крови известны давно. Использование методов аутогемотрансфузии или различное их сочетание позволяют сохранить необходимые клеточные и плазменные компоненты крови больного.
Кроме того, аутогемотрансфузия предупреждает заражение больных гепатитами, ВИЧ-инфекцией, цитомегаловирусной инфекцией и другими инфекционными заболеваниями. Аутотрансфузия исключает возникновение посттрансфузионных реакций и осложнений, даже при уже имеющейся сенсибилизации. Аутологичные эритроциты, собранные и обработанные в процессе операции, имеют преимущество в виде прямого, чаще немедленного использования без стандартных методов подбора.
Проблема аутогемотрансфузии разрабатывается в следующих основных направлениях: (1) предоперационная заготовка аутоплазмы, аутоэритроцитов и аутотромбоцитов; (2) интраоперационное резервирование аутокрови в сочетании с острой нормоволемической гемодилюцией; (3) сбор операционной крови и реинфузия аутоэритроцитов и (4) получение аутоэритроцитов из дренажной крови.
Среди указанных методик в клинической практике чаще используются предоперационная заготовка аутоплазмы и аутоэритроцитов и интраоперационная реинфузия аутоэритроцитов.
Показаниями к заготовке аутоплазмы в предоперационном периоде являются: (1) объём прогнозируемой кровопотери не более 1000 мл (не более 20% ОЦК); (2) предполагаемая в ходе оперативного вмешательства гипокоагуляция; (3) анемия (содержание Hb на уровне 100–120 г/л).
Противопоказаниями к заготовке аутоплазмы следует считать: низкое содержание общего белка менее 65 г/л и альбуминов менее 30 г/л; лёгочная и сердечно-сосудистая недостаточность, сепсис, септические состояния, ОРЗ, истощение, гемолиз любого генеза, хроническая почечная недостаточность с азотемией, печёночная недостаточность, выраженный атеросклероз, раковая кахексия, выраженный геморрагический синдром и тромбоцитопения (содержание тромбоцитов менее 50 000/мкл).
Методика получения аутоплазмы включает проведение, как правило, 2-этапного плазмафереза за 6–10 дней (1-я процедура) и 3–4 дня (2-я процедура) до операции с получением 800–1200 мл плазмы. При больших оперативных вмешательствах возможно получение за 10–30 дней до 2–3 л плазмы. В случаях сочетанного получения плазмы и тромбоцитов заготовку проводят за 1–2 дня до операции. Из аппаратуры чаще используют центрифуги типа ЦЛП 3–3,5 или аппараты для плазмафереза «Baxter» или «Haemonetics». Центрифугирование крови проводят со скоростью 2800 об/мин в течение 10 мин или 2200 об/мин в течение 15 мин.
В зависимости от состояния больного, исходного содержания общего белка и альбуминов, величины ОЦП рассчитывают объём получаемой аутоплазмы. Определение данной величины производят по специальным математическим формулам или с помощью отдельных номограмм. Принято считать, что содержание общего белка после плазмафереза должно быть не менее 60 г/л. Чаще осуществляют удаление 0,25% ОЦП. Плазмозамещение проводят введением стандартно 800–1000 мл 0,9% раствора хлорида натрия.
Реинфузия аутоплазмы в большинстве случаев выполняется в процессе операции, что обеспечивает стабильность коагулогических и гемодинамических показателей и белковых параметров.
Основными показаниями к заготовке аутоэритроцитов являются: (1) предполагаемая кровопотеря 1000–1200 мл (20–25% ОЦК); (2)трудности в подборе донорских эритроцитов; (3) трансфузионные реакции и (4) высокая опасность тромбоэмболических осложнений в послеоперационном периоде. Противопоказаниями к заготовке аутоэритроцитов могут быть: анемия (содержание Hb менее 120 г/л и величина гематокрита менее 30%), различные формы гемоглобинопатий, гипотония (АД менее 100/60 мм рт.ст.), сердечно-сосудистая декомпенсация, сепсис, септические состояния, ОРЗ, истощение, гемолиз любого генеза, печёночная недостаточность, почечная недостаточность с азотемией, раковая кахексия, выраженный атеросклероз, геморрагический синдром и тромбоцитопения (содержание тромбоцитов менее 50 000/мкл).
Алгоритм заготовки аутоэритроцитов включает:
— выполнение венепункции — инфузия 200–300 мл 0,9% раствора хлорида натрия — эксфузия расчётного объёма крови с учётом массы тела, исходного гематокрита и гемоглобина (как правило, не более 10% ОЦК у детей до 14 лет и пожилых больных старше 65 лет, обычно — 15% ОЦК);
— центрифугирование крови со скоростью 2400 об/мин в течение 10 мин;
— дополнительное введение хлорида натрия и ретрансфузия аутоплазмы.
За одну процедуру при выполнении двух эксфузий получают 200–450 мл эритроконцентрата. Оптимальный срок заготовки аутоэритроцитов до операции обычно составляет 5–8 дней при условии стабильности основных гемодинамических показателей, после заготовки аутоэритроцитов снижение гематокрита не допускается менее 30%, соответственно, уровня гемоглобина — менее 100 г/л.
Если потребность в эритроцитах превышает 15% ОЦЭ, которые нельзя заготовить за одну процедуру, применяют «прыгающий», или ступенчатый, метод. При каждом очередном получении одной дозы аутоэритроцитов с указанным интервалом ранее заготовленная эритроцитная масса переливается больному, а собираемая доза увеличивается. Таким образом, за короткое время можно заготовить до 1000 мл эритроцитов, которые обычно хранят в течение 5 дней.
При значительной кровопотере (более 1200 мл) проводится комбинированное ведение больного с использованием предоперационной заготовки аутоэритроцитов и выполнение интраоперационного сбора аутокрови. Существуют определённые методические подходы при использовании устройств и аппаратов для реинфузии. В экстренной хирургии сбор первого литра «спасённой» крови из грудной и брюшной полости, из малого таза проводят с помощью устройств для аутогемотрансфузии, позволяющих стабилизировать кровь, а затем её фильтровать. Дальнейший сбор аутокрови при таких операциях проводится на аппаратах для реинфузии с последующим центрифугированием такой крови и её отмыванием.
При выполнении ортопедических и нейрохирургических операций использование устройств для аутогемотрансфузии затруднено из-за тромбирования фильтров и невозможности выполнения отмывания аутоэритроцитов, поэтому реинфузия проводится в основном на аппаратах для реинфузии типа AT-1000 «Electromedics».
Абсолютными противопоказаниями к реинфузии аутокрови являются смешивание её с гнойным содержимым, смешивание крови с веществами, не предназначенными для в/в введения, и контаминация крови содержимым толстого кишечника. Относительными и, конечно, спорными противопоказаниями являются: смешивание крови с желчью, желудочным содержимым, околоплодными водами и простатической жидкостью. Проблематичной задачей применение реинфузии крови остаётся в онкологии. Перспективными направлениями в таких областях являются использование сорбционной технологии, интенсивного отмывания и фильтрации аутокрови через лейкофильтры.
15. ЭФФЕКТИВНОСТЬ ВОСПОЛНЕНИЯ КРОВОПОТЕРИ АУТОКРОВЬЮ ПРИ ВНЕМАТОЧНОЙ БЕРЕМЕННОСТИ
В. Е. Радзинский, И. М. Ордиянц.
Кафедра акушерства и гинекологии Российского университета дружбы народов, Москва, Россия.
Кафедра акушерства и гинекологии Российского университета дружбы народов, Москва, Россия.
Материнская смертность от внематочной беременности, несмотря на современные технологии диагностики и лечения, не имеет тенденции к снижению, а в так называемых развитых странах отмечено увеличение её последние 5–7 лет. Непосредственной причиной смерти в подавляющем большинстве случаев является геморрагический шок.
Ежегодный анализ случаев смерти от эктопической беременности в Российской Федерации постоянно выявляет две группы ошибок: диагностические и лечебно-тактические. Это, прежде всего неиспользование имеющихся стандартов диагностики эктопической беременности и отсутствие во всём мире стандартов восполнения кровопотери, особенно в больших количествах (1% и более от массы тела).
Современная диагностика трубной беременности и механизм её прерывания по типу разрыва трубы или трубного аборта, то есть экспульсия плодного яйца в брюшную полость, основаны на сонографическом поиске трофобласта вне матки и определении в крови и моче β-хорионического гонадотропина.
Таким образом, установление этих двух факторов даёт 100% диагностику до нарушения трубной беременности, что позволяет провести хирургическое лечение лапароскопически, бескровно и с сохранением в большинстве случаев маточной трубы как органа репродукции. К сожалению, в России 93% внематочных беременностей прооперированы при уже совершившемся разрыве трубы или при трубном аборте в ходу. Материнская смертность от внематочной беременности ежегодно составляет в среднем 5,7–7,2% всех случаев материнской смертности и занимает третье место в Структуре причин материнской смертности. Основной причиной смерти являются внутрибрюшное кровотечение и анестезиологические осложнения. Из умерших в стационаре от кровотечения 92,3% поступают в тяжёлом, крайне тяжёлом и агональном состоянии, что объясняется нарушением внематочной беременности, сопровождающейся массивным кровотечением до госпитализации. Геморрагический шок отмечен у 97%, ДВС-синдром — у 30%, острая почечная недостаточность — у 12%, клиническая смерть — у 13% умерших в стационаре.
Таким образом, в большинстве случаев неблагоприятные исходы при внематочной беременности обусловлены трудностями диагностики, поздней госпитализацией и, как следствие, — несвоевременным оперативным вмешательством. Кроме того, при данной патологии недостаточно осуществляется инфузионно-трансфузионная терапия, нередко из-за отсутствия крови и её компонентов.
Основной вопрос, возникающий перед хирургом и анестезиологом — целесообразность восполнения кровопотери и выбор трансфузионных средств.
В настоящем сообщении, основанном на почти пятнадцатилетнем исследовании возможностей инфузии аутокрови, предпринята попытка клинически обосновать использование аутокрови в случаях показанной гемотрансфузии.
За указанные годы аутоинфузия была проведена 711 женщинам, госпитализированным в гинекологическое отделение Республиканской клинической больницы им. Н. И. Пирогова в г. Ашхабаде (694 случая) и 17 женщинам в больнице №64 г. Москвы. Все женщины были прооперированы при наличии кровопотери различного объёма.
Следует отметить, что не только объём кровопотери определял необходимость гемотрансфузии, но и состояние больных, наличие у них белковожелезодефицитной анемии, как краевой патологии предшествующей беременности, и нестабильность гемодинамики.
В то время, когда мы активно внедряли аутоинфузии, побудительными мотивами были не боязнь СПИДа и даже гепатита, а элементарное отсутствие крови и её компонентов для восполнения объёма циркулирующей крови и объёма циркулирующей плазмы, поскольку национальные традиции и субэкстремальные климатические условия в сочетании с отсутствием холодильного оборудования не позволяли иметь необходимого запаса крови. Считая, что кровь в брюшной полости при внематочной беременности в силу своей несвёртываемости (она лишена фибрина) является удовлетворительной трансфузионной средой, мы в соответствии с накопленным в литературе опытом подготавливали её для инфузии путём фильтрации через 6–8 слоёв марли. При этом с 1984 г. до 1987 г. кровь забирали в стерильные флаконы с цитратом натрия, а с 1987 г., — с физиологическим раствором (50 мл) и 5 ед. гепарина.
Следует отметить, что ни в одном случае не было выраженных трансфузионных осложнений. Иногда требовалась дополнительная гемотрансфузия, как правило, при больших кровопотерях. До 1987 г. в качестве трансфузионной среды использовалась кровь, а с 1987 г. — эритромасса и замороженная плазма. Как и большинство хирургов, мы считаем нерациональным проведение аутоинфузии крови, излившейся в хирургическую рану. Вместе с тем уникальность крови в брюшной полости, не сворачивающейся в течение нескольких часов вследствие дефибринированности, отсутствия в ней антитромбина III, делает её незаменимой трансфузионной средой в случае отсутствия сведений о группе крови и резус-факторе, отсутствии эритроцитов, а также в силу общеизвестного факта 60% распространённости заболеваний, передающихся половым путём, в том числе СПИДа, многочисленных видов гепатита и туберкулёза.
До появления кислородпереносящих сред аутоинфузия крови при нарушенной трубной беременности будет занимать надлежащее место в системе жизнеобеспечивающих мероприятий, особенно в условиях недостаточной обеспеченности лечебных учреждений, в первую очередь, в сельской местности различным лабораторным оборудованием и препаратами донорской крови.
16. ВЛИЯНИЕ ПЕРЕЛИВАНИЯ КОМПОНЕНТОВ КРОВИ НА ВЕРОЯТНОСТЬ ПОВТОРНОГО КРОВОТЕЧЕНИЯ У БОЛЬНЫХ С ГАСТРОДУОДЕНАЛЬНЫМИ ЯЗВАМИ
Ю. В. Егоров, В. Н. Цыганков.
Кафедра госпитальной хирургии Российского университета дружбы народов, Городская больница №17, Москва, Россия.
Кафедра госпитальной хирургии Российского университета дружбы народов, Городская больница №17, Москва, Россия.
Проведён ретроспективный анализ 309 историй болезней с целью определить, уменьшает ли переливание плазмы (П) и эритроцитарной массы (ЭМ) в первые сутки пребывания больного в стационаре риск повторных кровотечений и оперативных вмешательств до 48 ч у больных с язвенными гастродуоденальными кровотечениями.
Больные от 22 до 72 лет, объём перелитой П и ЭМ был обусловлен имеющимися запасами в больнице и на станции переливания крови составил 250–600 мл. Степень кровотечения определялась на основании клинико-лабораторных данных по схеме, предложенной Ю. М. Панциревым и соавторами. Лёгкая степень соответствует кровопотере до 10% объёма циркулирующей крови (ОЦК), а глобулярного объёма (ГО) до 20%, средняя — 10–30% ОЦК и ГО, тяжёлая — свыше 30% ОЦК и ГО.
Частота возникновения повторного кровотечения и сроков оперативного вмешательства в течение 48 ч пребывания в стационаре не отличается от приводимой другими авторами и колеблется от 18% (А. И. Горбашко, С. М. Луценко и соавторы) до 35% (А. М. Ботвинов). Достоверно реже возникало повторное кровотечение у больных с кровотечением средней степени тяжести, которым переливали П или П и ЭМ, по сравнению с больными, которым гемотрансфузия не проводилась или переливали только ЭМ. Оперативное лечение достоверно чаше проводилось у больных с тяжёлой степенью кровотечения по сравнению с больными с кровотечением средней степени тяжести. Других достоверных различий не выявлено.
Переливание П не уменьшает риск повторного кровотечения у больных с кровотечением тяжёлой степени, что связано с недостаточной компенсацией потери плазменных факторов свёртывания. Считается (Lundsgaard-Hansen), что при потере 50% ОЦК возникает потребность в введении П, а при потере 80% — тромбоцитарной массы (что в наших условиях невозможно). Нет достоверных отличий в частоте повторного кровотечения между больными, которым переливали и не переливали П, в общем количестве больных. Поэтому главное, что определяет вероятность повторного кровотечения, — это его интенсивность (отличие достоверно), а не проводимая терапия. Это обусловлено невозможностью достаточного восполнения факторов свёртывания при массивной кровопотере, большим диаметром повреждённого сосуда, из-за чего не может образоваться устойчивый тромб.
Невозможность адекватно восполнить потерю факторов свёртывания и обеспечить достаточную газотранспортную функцию вследствие постоянно нарастающего дефицита компонентов крови при кровотечении тяжёлой степени определяет более активную хирургическую тактику, например К. И. Мышкин и соавторы рекомендуют при дефиците ОЦК более 800 мл (12%) экстренное оперативное вмешательство с восполнением возникших дефицитных состояний после оперативного вмешательства. В. Д. Братусь и соавторы отмечают, что летальность у больных с кровотечением тяжёлой степени, которым проводилась консервативная терапия, в 1,5 раза выше, чем после операции. До момента устойчивого гемостаза восполнение ОЦК целесообразно проводить кровезаменителями с минимальным влиянием на свёртывающую систему крови, которыми являются препараты гидроксиэтилированного крахмала (HES 200/0,5).
ЛИТЕРАТУРА
- [16:1] Ботвинов А. М. — Хирургия, 1980, № 7, С. 65–69.
- [16:2] Братусь В. Д., Фомин П. Д., Пацкань Б. М. и др. — Клин. хир., 1986, №8, С. 6–8.
- [16:3] Горбашко А. И. — Вестн. хир., 1980, № 9, С. 28–34.
- [16:4] Луценко С. М., Варвашеня В. М., Тихий А. К. и др. — Клин. хир., 1981, №4, С. 48–50.
- [16:5] Молчанов И. В., Гольдина О. А., Горбачевский Ю. В. Растворы гидроксиэтилированного крахмала — современные и эффективные плазмозамещающие средства инфузионной терапии. М., 1998.
- [16:6] Мышкин К. И., Боровский М. И., Франкфурт Л. А. — Хирургия, 1984, №9, С. 56–60.
- [16:7] Панцирев Ю. М., Сидоренко В. И., Орлов С. Н. и др. Основные вопросы лечебно-диагностической тактики при остром язвенном кровотечении из верхних отделов пищеварительного тракта. М., 1991.
- [16:8] Lundsgaard-Hansen P. Gibt es einen kritischen Hb-bzw. Hkt-Wert? // Anaesthesist, 1992, v. 41. — Supp. L.
17. ОЦЕНКА ЭФФЕКТИВНОСТИ ПЛАЗМОЗАМЕЩАЮЩЕГО ПРЕПАРАТА ГЕЛОФУЗИН В ИНТЕНСИВНОЙ ТЕРАПИИ ХИРУРГИЧЕСКИХ БОЛЬНЫХ
А. Е. Шестопалов, В. Г. Пасько.
Главный военный клинический госпиталь им. акад. Н. Н. Бурденко, Москва, Россия.
Главный военный клинический госпиталь им. акад. Н. Н. Бурденко, Москва, Россия.
Инфузионная терапия является одним из наиболее важных компонентов интенсивной терапии критических состояний у больных и пострадавших хирургического профиля, позволяющим в короткие сроки эффективно корригировать нарушенные функции организма. Вместе с тем эффективность инфузионной терапии во многом зависит от фармакологических свойств препарата и патогенетически обоснованной программы. Несмотря на наличие довольно большого арсенала средств инфузионной терапии, проблема разработки адекватных сред и совершенствования программ инфузионно-трансфузионной терапии остаётся в центре внимания исследователей и клиницистов.
В работе представлены результаты исследования эффективности применения препарата Гелофузин (4% изоонкотический, изотонический плазмозамещающий раствор на основе сукцинированного жидкого желатина, B. Braun, Германия) в программах инфузионной терапии волемических нарушений у 57 больных хирургического профиля в возрасте от 35 до 75 лет. В зависимости от характера гиповолемии и показаний к проведению инфузионной терапии с включением Гелофузина исследованные больные были разделены на три группы:
1-я группа — 27 больных с острой кровопотерей. Причина кровопотери — язвенная болезнь желудка и двенадцатиперстной кишки, осложнённая острым кровотечением;
2-я группа — 15 больных с ишемической болезнью сердца, которым перед началом операции АКШ выполняли заготовку аутокрови с адекватным восполнением объёма Гелофузином. Этим же больным Гелофузин (500 мл) применяли для заполнения аппарата искусственного кровообращения;
3-я группа — 15 больных общим перитонитом, у которых гиповолемия была обусловлена интоксикацией, тяжёлыми водно-электролитными и метаболическими нарушениями. При выборе состава и объёма инфузионно-трансфузионной терапии ориентировались на данные исследования объёма циркулирующей крови (ОЦК), гемоконцентрационные и биохимические показатели крови, системы гемостаза, КОС, центральной и периферической гемодинамики.
В 1-й группе у 17 больных (группа 1А) кровопотеря составила 15–17% ОЦК (700–900 мл), у 10 (группа 1Б) — 25–28% ОЦК (1600–1700 мл). Программа инфузионной терапии в группе 1А включала 40% Гелофузина и 60% растворов кристаллоидов с превышением объёма кровопотери в 1,5 раза; в группе 1Б — 30% Гелофузина, 20% растворов кристаллоидов, 20% свежезамороженной плазмы и 30% эритроцитарной массы с превышением объёма кровопотери в 2 раза. В последующем на 2-е–3-и сутки объём вводимого Гелофузина в среднем составлял 500–1000 мл/24 ч. Гемотрансфузия эритроцитарной массы на 2-е–3-и сутки не превышала 240 мл (группа 1А), а в группе 1Б — 320–400 мл.
Анализ полученных результатов показал, что до начала инфузионной терапии в группе 1А дефицит ОЦК по сравнению с должными величинами составил 9,3±2,9%; ГО — 30,3±3,5%. Артериальное давление было в среднем на уровне 100–110/60–65 мм рт.ст. Отмечали умеренную тахикардию с ЧСС 90–96 уд/мин. и снижение ЦВД до 32–35 мм вод.ст. Концентрация Hb не превышала 100–110 г/л, Ht 30–32%. В группе 1Б изменения волемических, гемодинамических и гемоконцентрационных показателей носили более выраженный характер. Так дефицит ОЦК составлял 14,7±1,8%; ГО — 38,5±4,9%. Артериальное давление в пределах 80–90/40–50 мм рт.ст.; ЦВД 20–26 мм вод.ст. ЧСС возрастала до 120–130 уд/мин. Показатели Hb 70–80 г/л и Ht 25–27% свидетельствовали о выраженной анемии.
На фоне проводимой инфузионной терапии у всех больных 1-й группы отмечено увеличение ОЦК (69–71 мл/кг) и ГО (23–26 мл/кг) с минимальным дефицитом ОЦК 2–3%, ГО 23–29% на 3-и сутки. Дефицита объёма плазмы на всех этапах исследования не выявлено. Стабилизация гемодинамических показателей отмечена сразу же после инфузии первых 500 мл Гелофузина и в последующем артериальное давление (120–130/70–80 мм рт.ст.), ЧСС 80–86 уд/мин и ЦВД 80–90 мм вод.ст. оставались в полосе физиологической нормы.
Таким образом, использование Гелофузина в сочетании с растворами кристаллоидов, альбумина, плазмы, эритроцитарной массы в применённых объёмах оказало хороший волемический и гемодинамический эффект, не вызвало существенных изменений свёртывающей системы крови (ПТИ 80–83%, фибриноген 3,09–3,24 г/л), электролитного баланса, кислотно-основного состояния, функционального состояния печени и почек.
Во 2-й группе при заготовке аутокрови в 6 случаях эксфузия крови составила 500 мл, инфузия Гелофузина — 500 мл; в 4 случаях объём эксфузии составил 1000 мл, инфузия Гелофузина — 1000 мл. Объём операционной кровопотери 10–15% ОЦК (645,3±85,2 мл). Время ИК 64,2±6,9 мин. Длительность операции 122,5±18,3 мин, анестезии 154,5±12,9 мин.
Анализ полученных результатов показал, что при нормоволемической гемодилюции Гелофузином до 500 мл возрастает ЦВД на 13,3% (52,8–59,1 мм вод.ст.), САД на 9,7% (74,5–81,7 мм рт.ст.), а величина гематокрита снижается на 39,7% (41,2–25,1 об%). В то же время при нормоволемической гемодилюции в объёме 1000 мл все указанные показатели снижаются: ЦВД с 54 до 37 мм вод.ст.; САД с 74 до 70 мм рт.ст.; Ht с 47,8 до 33,9%. Вместе с тем существенных изменений показателей центральной гемодинамики не выявлено.
Таблица 1.
| Показатели | До забора крови | После инфузии Гелофузина |
|---|---|---|
СИ, 1/мин/м2
|
2,13±0,199
|
1,92±0,014
|
УИ, мл/м2
|
34,6±2,9
|
34,1±1,8
|
ИОПС, dyne*S*м2/см5
|
2676,9±393,4
|
2979,5±251,8
|
ИРЛЖ, g*м/м2
|
30,3±2,28
|
29,46±1,15
|
ИРПЖ, g*м/м2
|
4,29±0,32
|
4,41±0,54
|
Это свидетельствует об отсутствии нагрузки на функцию миокарда, что также подтверждалось высокими показателями содержания кислорода в артериальной и венозной крови (PvO2 95–96 мм рт.ст., PaO2 128–130 мм рт.ст.). В целом полученные данные свидетельствуют о том, что при острой нормоволемической гемодилюции заполнение аппарата ИК Гелофузином обеспечивает эффективную коррекцию волемических нарушений без напряжения компенсаторных функций сердечно-сосудистой системы, поддерживает оптимальный уровень транспорта кислорода, адаптационных возможностей миокарда в условиях ИК у больных с ишемической болезнью сердца.
Инфузионная терапия послеоперационного периода больным 3-й группы в объёме 55–57 мл/кг/24 ч включала 30–35% Гелофузина; 30–35% растворы кристаллоидов; 5–7% 10% раствора альбумина; 7–9% свежезамороженной плазмы; 20% 10% раствора глюкозы. В последующем, как правило, со 2-х суток, в инфузионную терапию включали среды для парентерального питания (22–27 мл/кг/24 ч), соответственно уменьшая объём коллоидных и кристаллоидных препаратов. Средний расход Гелофузина в течение 3–4-х суток послеоперационного периода составил 500 мл/24 час.
Результаты выполненных исследований показали, что волемические нарушения в первые сутки после операции характеризовались уменьшением ОЦК с дефицитом 17,2±1,8 мл/кг за счёт дефицита как ГО (10,5±0,5 мл/кг), так и ОП (6,7±0,2 мл/кг). На фоне проводимой инфузионной терапии от 1-х к 5-м суткам прослеживается положительная динамика в увеличении ОЦК и уменьшении его дефицита до 5,5±0,2 мл/кг. Что касается компонентов крови, то их изменения были разнонаправленными. Так, если дефицит ГО в первые 2 сут составлял в среднем 8–9 мл/кг с последующей тенденцией к уменьшению до 6,5 мл/кг на 5-е сутки, то ОП на всех этапах наблюдения соответствовал должным величинам. Объём внеклеточной жидкости в течение 5 сут оставался равным должному. Полученные результаты свидетельствуют об адекватной коррекции волемических расстройств на фоне проводимой инфузионно-трансфузионной терапии. При этом нагрузка на сократительную способность миокарда не увеличивалась.
Таблица 2.
| Показатели | 1-е сутки после операции | 3-и сутки после операции | 5-е сутки после операции |
|---|---|---|---|
СИ, л*мин(м2)−1
|
4,4±0,1
|
3,02±0,65
|
3,22±0,52
|
РЛЖ, кгм/мин
|
2,1±0,1
|
2,25±0,07
|
2,13±0,06
|
Расход энергии, Вт
|
12,9±0,51
|
12,63±0,21
|
12,4±0,32
|
ОПС, дин. сек. см−5/м2
|
863,1±67,65
|
1064,0±175,1
|
1200,5±225,7
|
PaO2, мм рт.ст.
|
79,6±3,52
|
72,1±1,95
|
78,5±2,16
|
PvO2, мм рт.ст.
|
40,5±1,2
|
39,5±2,2
|
42,3±4,2
|
Более того, умеренный гипердинамический синдром — повышение сердечного выброса на 10–11% и работы левого желудочка на 57% без увеличения расхода энергии на фоне нормального ОПС и среднего давления в лёгочной артерии (24–26 мм рт.ст.) обеспечивал должный транспорт кислорода при компенсированной гиповолемии. Тем самым умеренная гипердинамия не сопровождалась напряжением компенсаторных функций миокарда, хотя исходно при перитоните сердечно-сосудистая недостаточность во многом обусловлена «истощением миокарда» гнойной интоксикацией, некардиальным интерстициальным отёком лёгких, микроциркуляторными нарушениями и высоким давлением в лёгочной артерии. Таким образом, можно полагать, что выполненная инфузионная терапия с включением препарата Гелофузин обеспечила в короткие сроки послеоперационного периода эффективную коррекцию волемических и гемодинамических нарушений у больных перитонитом.
В целом результаты выполненных исследований свидетельствуют о том, что применение препарата Гелофузин как коллоидного плазмозамещающего раствора в программах инфузионной терапии гиповолемических состояний различного генеза у больных хирургического профиля оказывает стойкий волемический и гемодинамический эффект. При этом основные показатели системы гемостаза не претерпевают существенных изменений и на всех этапах исследования остаются в физиологически допустимых пределах. Во всех случаях заготовки аутокрови и нормоволемической гемодилюции, первичного заполнения аппарата ИК Гелофузином каких-либо расстройств гемодинамики, анафилактических реакций, нарушений свёртывающей и антисвёртывающей систем, газового состава крови не отмечено.
18. КРОВЕСБЕРЕГАЮЩИЕ ПРИЁМЫ ПРИ СПЛЕНЭКТОМИИ У ГЕМАТОЛОГИЧЕСКИХ БОЛЬНЫХ
Г. И. Алексеев, Г. И. Веретник, А. С. Кириленко, В. Ю. Баранович.
Кафедра госпитальной хирургии Российского университета дружбы народов, Москва, Россия.
Кафедра госпитальной хирургии Российского университета дружбы народов, Москва, Россия.
Основным методом в лечении целого ряда больных с заболеваниями системы крови, а именно — с наследственной гемолитической анемией (НГА), аутоиммунной гемолитической анемией (АИГА), гипопластической анемией (ГА), парциально-красноклеточной аплазией (ПККА), хроническими миелопролиферативными заболеваниями (ХМЛ), хроническими лимфопролиферативными заболеваниями (ХЛЛ), лимфогранулематозом (ЛГМ), идиопатической тромбоцитопенической пурпурой (ИТП), является спленэктомия. В основу работы положен анализ результатов, полученных при проведении 1300 операций у больных с различными заболеваниями системы крови, оперированных в ЦКБ №2 МПС. Из этого количества в 1120 случаях выполнена спленэктомия, у 180 больных были произведены сочетанные операции (спленэктомия и холецистэктомия, резекция желудка, митральная комиссуротомия и др.).
Как одному из кровесберегающих факторов важное значение придавалось предоперационной подготовке, в основе которой было уменьшение степени анемии и ликвидация гиповолемии, терапия геморрагических осложнений, купирование гемолитического криза, адекватная кортикостероидная терапия, коррекция сахарного диабета и гипокалиемии, терапия воспалительных осложнений.
У гематологических больных само оперативное вмешательство представляет повышенный риск, в частности из-за нарушений свёртывающей системы. Отягощающими моментами, требующими особого внимания хирурга, являются резкая панцитопения, нарушение деятельности сердца и функции внешнего дыхания. В связи с применением цитостатических и гормональных препаратов снижается функция деятельности печени, надпочечников, иммунологическая резистентность организма. После спленэктомии вследствие удаления значительной части иммунокомпетентной ткани организма, как правило, развиваются клинические признаки иммунодефицита, что в свою очередь ведёт у оперированных больных к повышению частоты тяжёлых инфекционно-воспалительных осложнений — пневмоний, сепсиса, менингита, перикардита. Серьёзного внимания заслуживает присущее этим болезням нарушение гемостаза.
В общей хирургии спленэктомию принято считать достаточно простой операцией, но у гематологических больных она является не только сложной, но и опасной.
Существует большое число доступов к селезёнке. На основании нашего опыта мы пришли к заключению, что при удалении селезёнки средних размеров лучшие условия обеспечивает срединная лапаротомия. Основным преимуществом этого доступа является отсутствие необходимости пересечения мышечных массивов, что позволяет значительно снизить общую кровопотерю. Когда же необходимо удалить маленькую селезёнку у тучных больных, срединный доступ недостаточно удобен, так как не создаётся достаточной экспозиции, становится трудным выполнение ответственных моментов операции даже опытным хирургам. Хирургу приходится форсировать определённые этапы операции, что приводит к снижению её качества. В этих случаях предпочтение отдаётся доступу из косого разреза в левом подреберье.
Учитывая основной тяжёлый фон у этих больных, а именно, снижение гемостатических свойств крови, нарушение тромбообразования за счёт снижения форменных элементов крови, в частности тромбоцитов, возникают непредвиденные кровотечения из труднодоступных сосудов связочного аппарата селезёнки. Возможны обильные петехиальные кровоизлияния. Вследствие близкого анатомического расположения существует реальная опасность при спленэктомии повреждения хвоста поджелудочной железы. Кровотечение может возникнуть из серозного покрова желудка, кишечника, сдавленных крючками. Кроме того, перевязка сосудистой ножки селезёнки единым блоком у гематологических больных вследствие рыхлости ткани может привести к соскальзыванию лигатуры и обильному кровотечению и в более поздние сроки после операции. Поскольку снижено тромбообразование, принципиально важным кровесберегающим приёмом считаем раздельную перевязку сосудистой ножки селезёнки. При этом вначале перевязывается артерия, а спустя 3–5 мин — вена. Этот приём обеспечивает опорожнение селезёнки от собственной крови, что в целом сохраняет общий объём циркулирующей крови.
Таким образом, наш опыт проведения 1300 спленэктомий говорит о том, что наиболее трудными являются такие этапы операции: обработка коротких сосудов желудочно-селезёночной связки у верхнего полюса селезёнки, отделение селезёнки от брюшины и забрюшинного пространства; обработка сосудистой ножки селезёнки без повреждения хвоста поджелудочной железы. Тщательное выполнение всех этапов спленэктомии у гематологических больных, а также выбор рационального доступа являются кровесберегающими факторами, факторами уменьшения грозных осложнений у данной категории больных. Именно к такому высокопрофессиональному подходу — сбережению крови больного — должен стремиться каждый хирург чтобы уменьшить опасность, связанную как с кровопотерей, так и с переливанием донорской крови и тромбомассы.
Выводы:
Верхнесрединная лапаротомия значительно снижает операционную кровопотерю за счёт сохранения сосудов мышечного массива передней брюшной стенки, неизбежно повреждающихся при использовании традиционного косого разреза в левом подреберье.
В уменьшении общей кровопотери существенную роль играет последовательное раздельное лигирование вначале артерии селезёнки, а затем спустя 5–6 мин — вены.
Использование кровесберегающих приёмов значительно уменьшает число типичных для спленэктомии осложнений (панкреатит, парез желудочно-кишечного тракта, поддиафрагмальный абсцесс и др.).
19. МЕТОДЫ СБЕРЕЖЕНИЯ КРОВИ В АКУШЕРСКО-ГИНЕКОЛОГИЧЕСКОЙ КЛИНИКЕ
В. И. Кулаков, А. М. Абубакирова, Т. А. Фёдорова, И. И. Баранов, Т. С. Фотеева, О. В. Рогачевский, С. Г. Цахилова, В. Ф. Ковалёв.
Научный центр акушерства, гинекологии и перинатологии РАМН, Москва, Россия.
Научный центр акушерства, гинекологии и перинатологии РАМН, Москва, Россия.
В настоящее время развитие медицины и медицинской техники во многом изменили точку зрения на переливание крови и других трансфузионных сред. Технически просто выполнимое переливание крови и её компонентов сегодня рассматривается как сложнейшее иммунологическое воздействие, равное по значимости пересадке органов и тканей. Кроме этого необходимо помнить реально существующую опасность заражения пациента такими заболеваниями как СПИД, гепатит, герпес и пр. Усовершенствование знаний в области клинической трансфузиологии позволило пересмотреть показания к переливанию крови вплоть до отмены переливания цельной крови с использованием компонентов и препаратов крови по строго медицинским показаниям. В связи с этим, в настоящее время в клинической практике разрабатываются новые методы профилактики и лечения кровотечений, позволяющие избежать переливания донорской крови. Проблема кровотечения по-прежнему весьма актуальна в акушерско-гинекологической практике. Так, по данным ВОЗ, 63–80% случаев смерти прямо связаны с беременностью и родами, причём в 60–70% всех случаев смерти после или во время родов связаны с акушерскими кровотечениями. Причинами кровотечений являются различные осложнения во время беременности, родов и послеродового периода, обусловленные нарушениями прикрепления и отделения плаценты, сократительной деятельности матки, патологией системы гемостаза, эмболией околоплодными водами и т.д.
Также значительно возросла частота экстрагенитальных заболеваний, инфекционной патологии у акушерских и гинекологических больных. В последнее десятилетие количество первородящих в возрасте старше 30 лет возросло почти вдвое. Все эти факторы привели к увеличению оперативных вмешательств у акушерских больных, что, в свою очередь, ведёт к возрастанию таких грозных осложнений, как кровотечения и септические состояния. Сегодня пересматривается отношение к использованию консервированной крови как основного средства лечения кровопотери, так как при этом действуют определённые факторы риска: иммунологические, инфекционные, метаболические. Последнее десятилетие ознаменовалось значительным прогрессом трансфузиологии — освоением новых методов сбережения крови в периоперационном, в предродовом периоде. Трансфузионная терапия в настоящий момент требует особого внимания как со стороны врачей, так и со стороны административных кругов, ответственных за контроль использования препаратов крови. Появление специального соглашения — Европейской конвенции по правам человека и биомедицине — признак осведомлённости общественности о том, какими шагами идёт развитие медицины. Совет Европы, в частности, обратил внимание на вопрос переливания крови, подчеркнув важность «оптимального использования крови в соответствии с принципами её сбережения, как редкого и ценного вещества, с которым нельзя обращаться расточительно или неосмотрительно». В клинической медицине, в частности в акушерско-гинекологической практике, встаёт вопрос — можно ли ограничить использование чужеродной крови, не подвергая при этом больных неоправданному риску? Более того, для некоторых больных переливание крови невозможно по медицинским или религиозным причинам. Все эти факторы способствовали появлению возрастающего интереса к методам сбережения крови в акушерстве и гинекологии.
Методы сбережения крови в первую очередь направлены на поддержание уровня гематокрита, достаточного для обеспечения адекватного снабжения тканей кислородом. Адекватный предоперационный гематокрит, хорошая функция свёртывающей системы и применение методов сбережения крови в периоперационном периоде имеют важное значение. Дооперационный уровень гематокрита — важный прогностический фактор переливания крови. Это наводит на мысль об эффективности использования эритропоэтина перед операцией, особенно, если удастся снизить затраты и разработать более простые способы его введения. В связи с синтезом in vitro в 1985 г. эритропоэтического гормона — рекомбинантного эритропоэтина (РЭПО), появилась возможность эффективно и безопасно регулировать эритропоэз. Благодаря накопленному опыту применения РЭПО у больных с анемией различного генеза, прежде всего почечной, начались исследования, направленные на изучение результатов и перспектив применения РЭПО при анемиях у беременных, а также у гинекологических больных. Исследования показали, что назначение РЭПО перед родами, перед оперативным вмешательством позволяет избежать или, по крайней мере, снизить частоту гемотрансфузий у больных с анемией, число которых в акушерско-гинекологической клинике достаточно высоко. Так, в Москве и Санкт-Петербурге анемия выявляется у 40% беременных. Представляется, что применение РЭПО с целью стимуляции эритропоэза, особенно у больных с анемией — перспективное направление, требующее развития и позволяющее снизить частоту гемотрансфузий.
В последние годы с целью профилактики кровотечений у пациенток с высоким риском его возникновения в родах или при оперативном вмешательстве были предложены новые медикаментозные средства, увеличивающие коагуляционный потенциал крови, в частности транексамовая кислота (трансамча). Фармакологические свойства трансамчи основаны на:
(а) блокировании активатора плазминогена, что тормозит превращение последнего в плазмин, вследствие чего подавляется деградация фибрина плазмином. Антифибринолитическое действие ещё более усиливается при наличии в плазме антиплазминов, таких как альфа-2-макроглобулин;
(б) гемостатическом действии — препарат предотвращает фибринолиз, гипофункцию тромбоцитов, повышенную ломкость сосудов и увеличивает расход коагуляционных факторов. Помимо этого, трансамча оказывает антиаллергическое и противовоспалительное, подавляя плазмин, производящий кинин и активные пептиды, вызывающие аллергию и воспаление. Трансамча, снижая проницаемость сосудистой стенки, способствует исчезновению отёков, вызванных карригинином и брадикинином.
В НЦ АГиП трансамча применяется с профилактической и лечебной целью. С профилактической целью препарат используется при родоразрешении женщин, имеющих изокоагуляцию, не характерную для определённого срока беременности: при гипокоагуляции, болезни фон Виллебранда, идиопатической тромбоцитопенической пурпуре.
С лечебной целью препарат показан при следующих патологических состояниях: беременность в 1-м триместре, осложнённая хроническим ДВС-синдромом, антифосфолипидным синдромом, угрозой прерывания; беременность во 2-м триместре, осложнённая предлежанием плаценты, угрозой прерывания; ранний послеродовый период, осложнённый гипотонией матки.
Пристального внимания заслуживает предоперационная заготовка компонентов крови (аутогемо- и плазмодонорство), управляемая гемодилюция и интраоперационная реинфузия крови. При этих методиках отмечается улучшение микроциркуляции, транскапиллярного обмена, снижение процента тромбоэмболических осложнений, неосложнённое течение послеоперационного периода.
Предоперационная заготовка компонентов крови включает дозированный одно- или многократный забор крови или её компонентов до оперативного вмешательства с последующим их хранением и переливанием их во время операции. Заготовка цельной крови у беременных распространения не получила, хотя отдельные сообщения на эту тему имеются. При акушерских операциях организм женщины нуждается в возмещении факторов свёртывания, фибриногена, антитромбина III, которые потребляются в результате попадания в кровяное русло тромбопластических веществ и развития субклинических проявлений ДВС-синдрома. Основным донатором факторов свёртывания является свежезамороженная плазма (а также криопреципитат). В связи с этим имеет смысл дробная заготовка аутоплазмы. В НЦ АГиП РАМН осуществляется заготовка аутоплазмы методом прерывистого плазмафереза в количестве 600+50 мл за 2 забора с интервалом в 1 нед. На аутоплазмодонорство направляются беременные, планируемые на абдоминальное родоразрешение, а также пациентки с высоким риском развития кровотечения в родах или при оперативном вмешательстве. Показания для аутогемо- и плазмодонорства следующие:
— рубец на матке,
— многоплодная беременность,
— ОПГ гестозы,
— миома матки,
— предлежание плаценты,
— нарушения свёртывающей системы крови,
— пациенты с редкими группами крови (при невозможности подбора донорской крови).
Беременные должны быть соматически здоровы, уровень гемоглобина не ниже 90 г/л, гематокрит не менее 30%, эритроциты не менее 2,5 млн/мкл, общий белок не менее 60 г/л. Контроль за состоянием плода осуществляется методом кардиотокографии. Плазмовозмещение производится физиологическим раствором и реополиглюкином в соотношении 2:1. Хранение плазмы осуществляется при температуре −18°C.
Большие перспективы открывает методика криоконсервирования эритроцитов, которые могут храниться до 1 года, а при особых условиях — до 5 лет. В этих случаях создаётся банк аутокрови, которая может быть использована по мере надобности, т.е. у женщины до планируемой беременности забирают эритроциты, а при возникновении кровотечения во время родоразрешения — переливают. Однако в нашей стране данная методика широкого распространения не получила по экономическим причинам.
Управляемая гемодилюция была внедрена в клиническую практику в начале 70-х гг. Было показано, что высокий предоперационный гематокрит повышает риск послеоперационных осложнений, особенно тромбоэмболических.
Управляемая гемодилюция в режиме нормоволемии или гиперволемии показана при оперативных вмешательствах в гинекологии, так как эксфузия крови проводится до начала операции с последующим её возвратом во время операции или в раннем послеоперационном периоде и не может быть использована в акушерстве. При операции кесарева сечения многие авторы рекомендуют методику гиперволемической гемодилюции, сущность которой состоит в предварительном переливании растворов с высоким коллоидно-осмотическим давлением или осмолярностью, что даёт возможность коллоидам длительно удерживаться в сосудистом русле. Наиболее часто в качестве плазмозаменителей плазмы используют альбумин, декстраны, гидроксиэтилкрахмал. Преимущество метода заключается в улучшении микроциркуляции, в частности в маточно-плацентарной зоне, реологических свойств крови, в профилактике тромбозов и гнойно-септических осложнений, усилении лактации. Использование предоперационной гемодилюции снижает потребность в переливании крови на 18–100%. Есть данные, что этот метод имел 100% эффективность даже при сложных операциях на органах брюшной полости.
Наиболее перспективным представляется использование интраоперационной реинфузии крови. Первое клиническое применение реинфузии крови обычно связывают с именами лейпцигских хирургов Thies и Lichtenstein, которые впервые прибегли к нему при прервавшейся внематочной беременности. «Отныне ни одна женщина не должна умирать от разрыва маточной трубы во время операции, если используется реинфузия крови» — так была названа статья Lichtenstein, опубликованная в 1918 г. Надо отметить, что сообщения о применении реинфузии крови начали появляться ещё в XIX веке. Так в 1818 г. Blandell в Лондоне произвёл аутотрансфузию крови 10 женщинам, у которых было послеродовое кровотечение, 5 из них выжили. Эту методику впервые описал Хигмор в 1874 г. в журнале «Lancet». Кровь собирали в бутыли, фильтровали через слои марли и возвращали больному. В 1914 г. эту методику применили при операции по поводу прервавшейся трубной беременности. Известно, что в гинекологической практике при операциях по поводу внематочной беременности применяется простая методика, когда излившуюся в брюшную полость кровь фильтруют через несколько слоёв марли и переливают пациентке.
За рубежом до сих пор используют простые и экономичные системы для сбора крови не только во время операции, но и после неё — из дренируемых полостей. Однако в этом случае возникают проблемы, связанные с неотмыванием эритроцитов, переливанием свободного гемоглобина, тканевого детрита и прокоагулянтов, преимущественно тромбопластина. Но наиболее широкие перспективы открывает применение специальной аппаратуры для интраоперационной реинфузии крови. С появлением в 60-х гг. сепараторов крови начался новый этап в развитии реинфузии — появилась возможность отмывать собранные эритроциты аппаратным способом. Суть метода заключается в аспирации крови из операционной раны, отмывании эритроцитов физиологическим раствором при вращении в центрифуге и немедленном возврате эритровзвеси пациентке.
Преимущества аппаратного метода очевидны: удаляются продукты деградации фибрина и фибриногена, разрушенные или повреждённые клетки крови.
Аспирируемая кровь циркулирует по замкнутому контуру одноразовой системы, что обеспечивает её стерильность. Промывание физиологическим раствором снижает возможную бактериальную загрязнённость крови. Использование этого метода улучшает показатели гемостазиограммы в послеоперационном периоде, улучшает общее состояние больной. Отмывание эритроцитов существенно снижает уровень свободного гемоглобина, уменьшая тем самым риск возможной нефротоксичности реинфузируемых аутоэритроцитов. Необходимо отметить, что наличие в брюшной полости жидкостей типа фурацилина, небольших количеств спирта, йода, содержимого кист, не являются противопоказанием к реинфузии, ибо эти вещества будут отмыты во время промывания при высокой скорости вращения. Абсолютным противопоказанием к реинфузии служит наличие в брюшной полости кишечного содержимого, гноя. Относительным противопоказанием является наличие у больной злокачественного новообразования.
В последние годы идёт разработка использования реинфузии во время операции кесарева сечения, при этом необходимо помнить о наличии тромбопластических субстанций в околоплодных водах и возможности переноса их в сосудистое русло пациентки. Поэтому перед операцией у беременной целесообразно произвести амниотомию, использовать второй отсос непосредственно после извлечения ребёнка для аспирации околоплодных вод, сыровидной смазки и мекония. После этого можно использовать отсос для сбора крови и реинфузии, включая программу высококачественной отмывки эритроцитов с большим количеством раствора, что делает данную процедуру безопасной в акушерстве. Безусловно, далеко не каждая операция кесарева сечения требует применения интраоперационной реинфузии крови. В большинстве случаев достаточно предоперационной заготовки аутоплазмы. При расширении объёма оперативного вмешательства (консервативная миомэктомия, надвлагалищная ампутация и экстирпация матки), предлежании или низком расположении плаценты, преждевременной отслойке плаценты, варикозном расширении вен матки, гемангиоме малого таза данный метод, благодаря высокой эффективности, простоте выполнения и отсутствию осложнений, имеет большие перспективы в акушерстве. Основным препятствием для более широкого использования метода интраоперационной реинфузии крови является дороговизна импортного оборудования, что требует создания отечественных аппаратов.
Широкое внедрение в акушерско-гинекологическую практику современных методов сбережения крови, создание отделений переливания крови и экстракорпоральных методов терапии в крупных родовспомогательных и гинекологических учреждениях позволит значительно улучшить показатели здоровья населения, снизить материнскую и детскую заболеваемость, летальность от кровотечений и риск инфицирования женщины и ребёнка при переливании донорской крови.
20. ЦЕНТРЫ БЕСКРОВНОЙ МЕДИЦИНЫ — ПОЧЕМУ ВРАЧИ НАЧАЛИ ОБХОДИТЬСЯ БЕЗ ДОНОРСКОЙ КРОВИ
Доктор Мозес Б. Аджибойе.
Российский филиал Международной службы больничной информации Свидетелей Иеговы, Нью-Йорк, США.
(Перевод с английского.)
Российский филиал Международной службы больничной информации Свидетелей Иеговы, Нью-Йорк, США.
(Перевод с английского.)
В настоящее время в США существует более 100 центров бескровной медицины. Во всём мире проводится около 190 программ, направленных на сбережение крови. Какова же причина того, что накануне XXI века врачи всего мира вдруг стали ратовать за бескровные методы лечения, в то время как раньше «поклонялись» переливаниям? Быстрое увеличение количества медицинских центров и программ бескровной хирургии обусловлено рядом причин. Прежде всего — появление ВИЧ-инфекции, которое направило внимание врачей и общественности на необходимость поиска альтернатив крови. Вслед за этим обнаружение других инфекций привело многих специалистов к заключению, что переливания крови по своей сути представляют серьёзную опасность. Действительно, сегодня стало ясно, что безопасного переливания крови не существует. Также была обнаружена связь переливаний крови с инфекционными осложнениями. В клинических исследованиях было отмечено, что больные, получавшие переливание донорской или аутокрови, приблизительно в 4 раза чаще страдали инфекционными осложнениями по сравнению с теми, кто не получал переливаний. Все эти данные способствовали развитию бескровной медицины.
Более того, в связи с повышением затрат, связанных с необходимостью дополнительного тестирования донорской крови, было подсчитано, что реальная стоимость одной упаковки крови (учитывая кроме непосредственной стоимости затраты на лечение возможных осложнений) может оказаться равной 1000 $.
Кроме вышеуказанного, были разработаны новые медицинские приборы, развиты новые усовершенствованные технологии и лекарственные средства. Всё это также стало составными частями понятия «бескровная медицина». Результаты превзошли ожидания. Несмотря на то что контролируемых исследований пока не проводилось, были собраны данные из 16 медицинских журналов, в которых описывались хирургические вмешательства у больных, принадлежащих к религиозной общине Свидетелей Иеговы (операции, при которых обычно используется переливание крови, им проводили без переливаний). Полученные результаты поддерживают концепцию о том, что всего лишь 0,5–1,5% таких операций осложняются анемией, которая в отсутствие лечения может привести к смерти. Таким образом, прогнозируемый риск отказа от переливания крови следует оценивать с учётом стоимости, риска осложнений и смертности, которые могут иметь место при использовании препаратов крови.
Бескровная медицина — это не только отказ от назначения донорской крови. Для врача это означает знания и опыт применения альтернативных методов. Использование донорской крови и её компонентов можно ограничить или устранить благодаря систематическому, комплексному и своевременному использованию лекарственных средств, доступного оборудования, а также хирургических и нехирургических методик. Именно такой комплексный подход обеспечивает выраженный сочетанный эффект. Применению альтернативных методов способствует выработка комплексного плана ведения больного в течение всего периода лечения. Использование альтернативных методов для интенсивной терапии тяжёлой анемии будет способствовать повышению качества лечения. Это требует непрерывного повышения квалификации — в теоретическом и практическом отношении.
Бескровные методы становятся своего рода «золотым стандартом». Такой подход способствует обеспечению права больного на принятие самостоятельных решений и неприкосновенность своего тела, а также помогает уменьшить или устранить конфронтацию и судебные иски. Да, завтрашний день пришёл к нам в виде центров и программ бескровной медицины.
ПРИЧИНЫ ПОЯВЛЕНИЯ И ДОСТОИНСТВА БЕСКРОВНОЙ МЕДИЦИНЫ
(×) Использование препаратов крови дорого, опасно и может заканчиваться летально.
(×) Рост нехватки донорской крови в национальных и мировых масштабах.
(×) Общественность, в связи с повышением осведомлённости об опасностях донорской крови, требует использования бескровных методов.
(×) Наличие альтернативных методов. Новые аппараты, новые и усовершенствованные методики, а также новые лекарственные препараты дают возможность проведения бескровных программ. Использование этих методов не сопровождается достоверным повышением летальности и осложнений.
(×) В целом, применение бескровных методов более экономично.
(×) Способствует повышению врачебной квалификации и мастерства. Даёт возможность делать собственные открытия.
(×) Обеспечивает наличие больных для проведения научных клинических исследований.
(×) Способствует обеспечению права больного на принятие самостоятельных решений и неприкосновенность своего тела — прекрасный метод устранения конфронтаций, недовольства и судебных исков.
(×) Способствует известности клиники.
21. УСПЕШНЫЕ ОПЕРАЦИИ НА СЕРДЦЕ БЕЗ ПЕРЕЛИВАНИЯ КРОВИ
М. Эстиоко, MD.
Клиника Good Samaritan, Лос-Анджелес, Калифорния, США.
(Перевод с английского.)
Клиника Good Samaritan, Лос-Анджелес, Калифорния, США.
(Перевод с английского.)
При хирургических вмешательствах без переливания крови, исключающих связанный с переливанием риск, вполне можно рассчитывать на успех. Главным фактором здесь служат вопросы свёртываемости крови и тщательного гемостаза. Бескровные операции на сердце привлекают широкое внимание, поскольку неприменение крови полезно во всех отношениях: предотвращаются не только осложнения, вызванные передающимися с кровью болезнями, но и, хочу подчеркнуть, проблемы, связанные с действием самой перелитой крови. Было показано, что переливание крови отрицательно сказывается на иммунной системе пациента, подвергая его большему риску инфекции и делая более восприимчивым к злокачественным и иным опухолям. Смысл появления бескровной хирургии заключался в том, чтобы сократить передачу инфекций с кровью, а также удовлетворить просьбы пациентов, которые не принимали переливания чужой крови в силу религиозных убеждений. В дальнейшем были обнаружены другие преимущества этого направления — больные остаются в клинике меньше времени, снижаются денежные затраты, исключаются связанные с переливанием осложнения, в частности (ставшее известным не так давно), подавление иммунной системы.
Появлению бескровной хирургии способствовал прогресс в различных областях медицины — новая медицинская аппаратура, усовершенствованные методики и лекарственные средства. Методика, состоящая из семи этапов, которая была разработана нами, позволяет безопасно и успешно проводить операции на сердце без переливания крови. Сюда входит:
— повышение гематокрита больного в процессе предоперационной подготовки;
— сведение кровопотери к минимуму при помощи тщательнейшей хирургической техники;
— контролируемая гемодилюция с использованием аппаратов искусственного кровообращения, имеющих небольшой заполняющий объём, и наполненных кристаллоидным раствором;
— назначение точно рассчитанных количеств гепарина и протамина сульфата;
— возвращение в организм после операции всего перфузата;
— назначение факторов свёртывания;
— правильный уход за больным в послеоперационном периоде, направленный на профилактику кровотечения.
Рассмотрим один пример. Больная 57 лет страдала артериальной гипертонией, сахарным диабетом и гиперлипидемией. Она была доставлена в одну из клиник с жалобами на боль в груди и одышку. Был поставлен диагноз: сердечная недостаточность на фоне ишемии миокарда. Физикальное исследование и катетеризация сердца выявили ишемическую болезнь с поражением трёх крупных стволов коронарных артерий. У больной была анемия (уровень гемоглобина составлял 100 г/л, а гематокрит — 33%). Для стимуляции выработки эритроцитов в течение четырёх недель проводилось лечение препаратами железа и эритропоэтином. Как показывает наш опыт, применение во время операции таких препаратов, как апротинин и эпсилон-аминокапроновая кислота, сокращает кровопотерю и устраняет необходимость в переливании крови. Эритропоэтин назначался чтобы увеличить массу эритроцитов и повысить уровень гемоглобина.
Один из главных факторов, обуславливающих необходимость переливания, — это гематокрит. Поэтому важно, чтобы показатели красной крови были в норме или даже несколько выше. Это достигается при помощи эритропоэтина, особенно если у больного исходно имеется анемия. Тщательный гемостаз играет важнейшую роль в расчёте предполагаемой кровопотери. По нашему мнению для гемостаза и наименьшего повреждения тканей хорошо подходят такие современные аппараты, как аргонный лазерный коагулятор, применяемый одновременно с электрокаутеризацией. В настоящее время мы проводим апробацию аргонного лазерного коагулятора под названием «Con-Med». Аргонный лазерный коагулятор обеспечивает надёжную остановку кровотечения в любой точке грудной полости. Область разреза остаётся сухой, кровотечения нет — всё это за счёт тщательного гемостаза на каждом этапе операции. Принцип действия аргонного лазерного коагулятора заключается в эффективном рассеивании радиоволновой энергии с помощью аргона, инертного газа, в результате чего повышается эффективность гемостаза. Ткани затрагиваются лишь поверхностно, и, как я уже упомянул, меньше повреждаются. Судя по предварительным данным исследований с применением аргонного лазерного коагулятора, метод даёт хорошие результаты. Удаётся значительно сократить число переливаний крови при первичных операциях коронарного шунтирования и операциях на клапанах сердца.
При использовании искусственного кровообращения, чтобы предотвратить чрезмерное разведение крови, крайне важен аппарат с низким заполняющим объёмом, а также ограничение в/в инфузии жидкости до, во время и после искусственного кровообращения. Это позволяет избежать коагулопатии, к которой приводит чрезмерное разведение факторов свёртывания, а во время операции проще поддерживать гематокрит. Насос для нагнетания крови в аппарате «сердце-лёгкие» мы заменили на насос-центрифугу (мы используем насос-центрифугу «3M Snars»). Это более эффективный и управляемый метод (по сравнению с роллерным насосом, который использовался многие годы). Не менее важно и то, что насос-центрифуга подаёт кровь пульсирующим потоком, напоминающим естественный, что значительно лучше непульсирующего потока, производимого старыми насосами. За счёт этого во время искусственного кровообращения улучшается гемодинамика, меньше страдают клетки крови и факторы свёртывания. Для дальнейшего сокращения объёма заполняющего раствора во время искусственного кровообращения трубки аппарата «сердце-лёгкие» были укорочены, а аппарат помещён ближе к больному.
Даже не говоря об осложнениях, связанных с переливанием донорской крови, бескровные операции экономически выгодны, поскольку сама по себе подготовка и обработка препаратов крови стоит денег. Лечение же осложнений, вызванных многочисленными переливаниями крови, обходится ещё дороже. После операции пациенты поправляются быстрее, в чём также проявляется рентабельность бескровной хирургии. Больные выписываются через 4–5 дней.
Мы провели сотни операций на открытом сердце без переливания крови. У более 500 пациентов, отказавшихся от переливания по религиозным причинам, результаты были великолепны. Срок их пребывания в отделении кардиохирургии был значительно короче, меньший срок требовалась искусственная вентиляция лёгких. Ещё раз хочу подчеркнуть, что по сравнению с ними другие прооперированные пациенты остаются в больнице гораздо дольше. Мы постоянно фиксируем всю информацию и ведём статистику, которая доказывает экономичность метода.
Известно, что повторные операции опасны кровотечением. Тем не менее, лишь одна из 22 повторных операций на сердце, проведённых нами без переливания крови, сопровождалась летальным исходом (причём, не связанным с кровопотерей). Таким образом, летальность составила 4,5%. Согласно сообщениям, при аналогичных операциях смертность может достигать более 25%.
57-летняя пациентка, о которой говорилось выше, уже полностью поправилась и чувствует себя хорошо. Бескровная хирургия — это хирургия сегодняшнего и завтрашнего дня. Её успех объясняется самим подходом: предоперационная подготовка пациента, тщательное планирование и тщательный гемостаз в течение операции. Не менее важен и послеоперационный уход за больным. Хирургическая бригада должна состоять из квалифицированных специалистов, постоянно совершенствовать методы работы, использовать современное оборудование, а также — что немаловажно — избегать консервативного мышления. Итак, бескровная хирургия послужит всем только на благо, поскольку её превосходные результаты налицо.
22. ТОЛЕРАНТНОСТЬ К АНЕМИИ. СТРАТЕГИЯ БЕСКРОВНОЙ ХИРУРГИИ — РОЛЬ АНЕСТЕЗИОЛОГА
А. Шандер, MD.
Центр бескровной хирургии клиники Инглвуд, Нью-Джерси, США.
(Перевод с английского.)
Центр бескровной хирургии клиники Инглвуд, Нью-Джерси, США.
(Перевод с английского.)
ВВЕДЕНИЕ
В докладе будут рассмотрены следующие вопросы — респираторная функция гемоглобина; роль гемоглобина, как средства доставки O2тканям; концепция о том, что уровень гемоглобина служит показанием к переливанию крови, осложнения и недостатки гемотрансфузии, а также ряд методов ведения больных, находящихся в критическом состоянии.
Прежде всего, гемоглобин — это переносчик кислорода. Обычно мы рассматриваем его как главное средство доставки O2 тканям. При каком уровне гемоглобина следует назначать переливание крови? Этот показатель так же неуловим, как источник молодости. Мы постоянно ищем это магическое число, которого не существует вообще. Непростые вопросы, связанные с определением объёма циркулирующей крови, острой нормоволемической гемодилюцией, показывают насколько сложна эта проблема.
Несколько слов о необдуманном использовании крови. Обычно в медицине стараются избегать методов лечения, недостаточно обоснованных в научном отношении, стараясь применять либо явно целесообразные, либо подтверждённые наукой способы. Однако решение о трансфузионной терапии почему-то оставлено на усмотрение лечащего врача, который, назначая её, едва ли следует какой-либо системе. Когда речь заходит о преимуществах донорской крови, её опасности подсознательно воспринимаются как менее значительные. Я же буду рассматривать вопрос с точки зрения конечных результатов.
РОЛЬ ГЕМОГЛОБИНА
«Основной мотив, от которого зависит решение — переливать или не переливать эритроциты — заключается в том, что они служат переносчиками кислорода от лёгких к тканям через систему микроциркуляции». В этом утверждении не учтён ряд существенных пробелов в знаниях о крови и её респираторной функции. Простота этой системы преувеличена. Как я уже говорил, долгие годы широкий путь принимают за истинный. Некоторые считают, что потребление O2 полностью зависит от его доставки. Теперь мы понимаем, что это лишь часть действительности и далеко не всегда соответствует описанному механизму. Показано, что переливание эритроцитов, хранившихся 28 дней в цитратно-фосфатно-декстрозо-адениновом растворе, не смогло улучшить насыщение тканей кислородом. Это исследование состояло из нескольких этапов. У 37 крыс имитировали оперативные вмешательства. У трети животных кровь хранили 3 сут, затем — переливали обратно. Остальным кровь переливали после 28 сут хранения. Результаты: (1) использование крови, хранившейся 28 сут, не повлияло на системное потребление O2; (2) повышение уровня гемоглобина не изменяло насыщения тканей кислородом.
Транспорт O2 гемоглобином представляет собой сложную систему, обладающую огромным резервом. Её регуляция и механизмы на микроциркуляторном уровне неизвестны. Доставка O2 напрямую зависит от способности крови переносить его. Резервы этой системы настолько велики, что гипоксия проявляется лишь при значительном снижении доставки O2. Кроме нелинейной зависимости насыщения тканей кислородом, одного из самых важных показателей для решения вопроса о переливании, в работе этой системы принимают участие другие неучтённые факторы, о существовании которых мы пока не знаем. О её сложности, в частности, свидетельствует недавно описанная зависимость работы генов от реакции клеток на гипоксию. В клетках обнаружен фактор, названный HIF-1 (фактор, индуцируемый гипоксией), который в ответ на гипоксию вызывает экспрессию генов, влияющих на развитие кровеносных сосудов и их расширение, эритропоэз, дыхание, синтез гликолитических ферментов для анаэробного пути метаболизма.
Следующий фактор, на который стоит обратить внимание, это роль окиси азота (NO), связанной с молекулой гемоглобина. Эритроциты используют NO в качестве посредника, который обнаруживает ткани, слабо насыщенные кислородом. При высвобождении NO расширяются капилляры, это позволяет эритроцитам избирательно доставить O2 в ткани, где его недостаточно. Благодаря этим знаниям становится понятно, как выживают больные с уровнем гемоглобина ниже критического.
Другая особенность гемоглобина состоит в том, что он влияет на кровоток. Оказалось, что эритроциты лучше всего протискиваются через капилляры при низкой концентрации гемоглобина. Так, исследования среди больных диабетом, перенёсших пластику сосудов нижних конечностей, показали, что при низком уровне гемоглобина проходимость сосудов лучше, чем при высоком.
Движение крови по сосудам происходит в соответствии с законами физики — не так упрощённо, как мы это представляем. Согласно принципу Бернулли, в центре сосуда кровь движется быстрее, чем вдоль его стенок. Применяя этот принцип к большому кругу кровообращения, можно заметить, что скорость движения плазмы вдоль стенок сосуда меньше, чем у эритроцитов, которые продвигаются в центре. Из-за этого концентрация плазмы по сравнению с концентрацией эритроцитов возрастает, и гематокрит в сосудах снижается. В большей степени это справедливо для микроциркуляции, чем для крупных сосудов. Таким образом, в микроциркуляторном русле гематокрит может быть примерно на 33% ниже, чем в крупных сосудах.
КРИТЕРИИ ДЛЯ НАЗНАЧЕНИЯ ГЕМОТРАНСФУЗИИ
Критический уровень гемоглобина — единственное общепринятое основание для переливания эритроцитов. Традиционно этот показатель считали равным 10 г% (Ht 30%), а в настоящее время — 7–8 г% (Ht 21–24%). Как уже говорилось, при решении вопроса о переливании крови, наиболее часто опираются только на уровень гемоглобина. Однако следует обращать внимание на объём циркулирующей крови (абсолютный ОЦК). Представим себе двух человек: один — непосредственно после острой кровопотери, другой — контрольный. Уровень гемоглобина у обоих одинаков, но ОЦК значительно отличается.
Почему же, тогда, мы так полагаемся на этот показатель? Дело в том, что объём крови очень трудно измерить, а для того, чтобы идентифицировать и подсчитать клетки крови требуется время. Недавно был сконструирован новый счётчик радиоактивных частиц с коротким периодом полувыведения, скоро начнётся IV период его испытаний. С помощью этого счётчика ОЦК можно будет определить примерно за 4 минуты.
Острую нормоволемическую гемодилюцию (ОНГ) — метод, позволяющий избежать большой кровопотери — одновременно можно использовать, как своеобразную «модель» анемии. С практической точки зрения эта методика требует от врача хорошего понимания физиологии. Общепринятых нормативов её контроля пока нет. Мы решили контролировать ОНГ при помощи измерения основных физиологических показателей. Были получены интересные результаты. Например, риск сердечных осложнений всегда тесно связывали с уровнем гемоглобина. Однако ни у одного из наших больных не было таких осложнений, поскольку у них поддерживали нормальный ОЦК. Carson в журнале Lancet сообщал, что сердечные осложнения можно прогнозировать в зависимости от уровня гемоглобина. Оказалось, что при проведении этих исследований не учитывали ОЦК. Если мы будем следовать подобной логике и лечить симптомы заболеваний сердца опираясь лишь на уровень гемоглобина, а не на подлинные патогенетические механизмы этих заболеваний, то после переливания крови у больного (независимо от уровня гемоглобина) неизбежно появятся боли за грудиной. Количество проведённых гемодилюций в нашей клинике равномерно увеличивалось с 1994 г., все они сопровождались прекрасными результатами. При гемодилюции (уровень гемоглобина снижали от 14,0 до 7,0 г%), независимо от количества забранных единиц крови, не наблюдалось значительных изменений систолического и диастолического давления или ЧСС.
Для оценки реакции сердечно-сосудистой системы и метаболизма на острую тяжёлую изоволемическую анемию были проведены исследования, недавно опубликованные в JAMA. У 11 больных в предоперационном периоде и у 21 оплачиваемого добровольца забирали от 450 до 900 мл цельной крови. В итоге уровень гемоглобина не превышал 5,0 г%. Как оказалось, если ОЦК был восстановлен до нормы, то независимо от уровня гемоглобина, уровни лактата и системной доставки кислорода не изменялись. При снижении уровня гемоглобина сердечный индекс возрастал. Предполагают, что это направлено на компенсацию анемии за счёт относительного увеличения ЧСС, а, следовательно, и минутного объёма. Согласно нашим исследованиям ЧСС несколько возрастала, но не отражалась на сердечном индексе.
Д-р Corwin из Дартмута, д-р Hebert из Канады, а также итальянские исследователи показали, что смертность тяжёлых больных может быть тесно связана с гемотрансфузиями. При переливании крови больным с ИБС летальность может расти. 69 больных (у которых поддерживалась нормоволемия) были разделены на две группы. В одной группе гемоглобин поддерживали на уровне 10–12 г%, при необходимости назначая переливание эритроцитов. В другой, этот порог был ниже (7–9 г%). Анализ показателей летальности за период 120 сут показал, что выживаемость и риск нарушения функции органов не зависели от переливания препаратов крови. Д-р Hebert в личной беседе сообщил, что при анализе исходов у 850 больных, находившихся в отделении интенсивной терапии, была видна явная взаимосвязь между летальностью и переливанием препаратов крови.
Медицинские работники использовали кровь в качестве лекарственного средства — «препарата» для лечения состояния, называемого анемией. При этом не проводилось никаких испытаний (I, II, III фаз) и дорогостоящих исследований. Для использования крови нет чётко сформулированных показаний. Возникают вопросы: если кровь — ткань, как можно её трансплантировать без строгих показаний? Кто может это назначить? Кто должен это фиксировать и строго контролировать? Ведь кровь, как и любой другой орган, имеет многочисленные функции — большие компенсаторные резервы, волшебные свойства, вид, запах, особый вкус и огромные возможности для регенерации. В США и в большинстве стран мира, когда дело касается крови и её применения, врачи ведут себя одинаково. Все мы виноваты в том, что на кровь смотрят как на лекарственное средство, а не как на орган. Чем больше накапливается информации, тем больше мы осознаём, что наши знания об этом органе весьма ограничены. В соответствии с заключением согласительной комиссии Национального института здравоохранения США (1988 г.), будь кровь лекарственным препаратом или органом, критериев для её переливания недостаточно. До 1987–88 гг., когда собралась первая согласительная комиссия, не предпринималось никаких попыток пролить свет на эту проблему. И хотя рекомендации этой комиссии весьма разумны и по сей день не утратили значения, к ним обращаются очень редко.
ОСЛОЖНЕНИЯ И НЕДОСТАТКИ ГЕМОТРАНСФУЗИИ
Неблагоприятные факторы, связанные с гемотрансфузией, включают: инфекции, подавление иммунитета, нехватку крови и недостаточный эффект от её применения.
Известно, что после переливания донорской крови нередко возникают инфекционные осложнения, могут реактивироваться латентные инфекции, в течение многих лет наблюдаются нарушения иммунитета. Подавление иммунной системы проявляется, в частности, в следующем: после трансплантации почки или других органов переливание крови улучшает жизнеспособность трансплантата; повышается риск метастазирования и рецидивирования злокачественных опухолей.
Нехватка препаратов крови становится проблемой в США и Европе. Только 5% населения США являются донорами. О нехватке крови также сообщают из Африки. Кроме того, в связи с увеличением продолжительности жизни растёт число реципиентов. Пока не появятся недорогие искусственные переносчики кислорода, проблема нехватки крови будет всё более усугубляться. Таким образом, сбережение крови и применение бескровных методов лечения может значительно помочь в решении этой проблемы.
По мере того, как мы бьёмся над снижением опасностей донорской крови, складывается впечатление, что её преимущества весьма сомнительны. С какой целью назначают гемотрансфузию? Чтобы увеличить доставку кислорода, улучшить тканевой метаболизм, устранить ряд симптомов и восполнить объём потерянной крови. Консервированная кровь в определённой степени теряет жизнеспособность и может быть опасна для больного. В ней исчезает важное вещество — 2,3-ДФГ (дифосфоглицерат), для восстановления которого требуется несколько часов. В течение этого срока система доставки кислорода действует очень плохо. Кроме того, перелитая кровь может повлиять на реологию и создать дополнительные препятствия для транспорта кислорода. При хранении на холоде эритроциты теряют эластичность и хуже проходят через капилляры, что приводит к тканевой гипоксии. Консервированная кровь может утрачивать способность использовать NO в качестве посредника. В отсутствие NO, который перераспределяет поток крови в участки, лишённые кислорода, кровь будет поступать в богатые кислородом ткани. Неблагоприятные последствия этого явления для больных с ИБС уже упоминались.
Известно, что при хронической анемии состояние больных полностью компенсировано. Таким образом, симптомы заболевания могут быть связаны в первую очередь с падением ОЦК, а не уровня гемоглобина. Для того, чтобы лучше понять это, в настоящее время ведутся исследования больных с анемией на фоне онкологической патологии и ВИЧ-инфекции.
ПРИНЦИПЫ ЛЕЧЕНИЯ БЕЗ ПРЕПАРАТОВ КРОВИ
(1) Подготовка
Надо действовать в соответствии с обстоятельствами, а не цифрами. Необходимо учитывать многочисленные альтернативные методы, а также опасности, которым подвергает больного переливание донорской крови. К методам, позволяющим обойтись без донорской крови, относятся: аутогемотрансфузия (переливание аутокрови); снижение интраоперационной кровопотери; ОНГ; использование переносчиков кислорода, препаратов, улучшающих гемостаз и рекомбинантных лекарственных средств.
Какими принципами должен руководствоваться хирург, имеющий цель предотвратить кровопотерю?
(1) Должен быть готов к сотрудничеству.
(2) Своевременно выявлять и обследовать больных с нарушениями свёртывания.
(3) При риске кровотечения оперировать как можно скорее.
(4) Использовать предоперационную эмболизацию.
(5) Составить план, выделив основные этапы операции.
(6) Применить доступные методы сбережения крови.
(7) По возможности свести к минимуму инвазивные манипуляции.
(8) Использовать для рассечения тканей ультразвуковой нож и подобные приспособления.
(1) Должен быть готов к сотрудничеству.
(2) Своевременно выявлять и обследовать больных с нарушениями свёртывания.
(3) При риске кровотечения оперировать как можно скорее.
(4) Использовать предоперационную эмболизацию.
(5) Составить план, выделив основные этапы операции.
(6) Применить доступные методы сбережения крови.
(7) По возможности свести к минимуму инвазивные манипуляции.
(8) Использовать для рассечения тканей ультразвуковой нож и подобные приспособления.
Возможно ли эффективно предотвратить острую анемию при хирургическом вмешательстве? Если мы объединим усилия, то сможем значительно снизить или полностью отказаться от использования донорской крови.
(2) Лекарственные средства
Рекомбинантные препараты (эритропоэтин; колониестимулирующие факторы роста гранулоцитов, макрофагов, мегакариоцитов; факторы свёртывания). Некоторые из этих препаратов есть в наличии, что снижает потребность в переливании препаратов крови.
Гемостатические препараты (аминокапроновая кислота, транексамовая кислота, апротинин, десмопрессин, вазопрессин, местные кровоостанавливающие средства [Avitene, Gelfoam, Surgicel, фибриновый клей], витамин K). Показано, что эти препараты в состоянии снизить потребность в препаратах крови у больных с желудочно-кишечным кровотечением, при операциях на сердце и ортопедических операциях, а также при некоторых нарушениях свёртывания.
(3) Тактика при тяжёлой анемии
(×) Немедленная остановка кровотечения
(×) Диагностика нарушений свёртывания
(×) Интраоперационная аутотрансфузия
(×) Введение соответствующих лекарственных средств (см. выше)
(×) Введение седативных препаратов, миорелаксантов и начало ИВЛ
(×) Парентеральное питание и введение препаратов железа
(×) При выраженной анемии — гипербарическая оксигенация
(×) В отсутствие эффекта, для стимуляции эритропоэза назначают препараты андрогенов.
При развитии тяжёлой анемии у больных, которым переливание крови по тем или иным причинам противопоказано, следует провести все вышеперечисленные мероприятия. Категорически запрещается любое промедление — важно действовать!
НАШ ОПЫТ
Больные, которые пользовались программой бескровного лечения в нашей клинике (1994–1998 гг.)
| Год | Число больных | Летальность |
|---|---|---|
1994
|
510
|
0
|
1995
|
650
|
1 (0,15%)
|
1996
|
1057
|
1 (0,09%)
|
1997
|
1267
|
1 (0,08%)
|
1998
|
1949
|
3 (0,15%)
|
Среди выживших за этот срок был 1 пациент с уровнем гемоглобина 1,7 г%, 5 — с уровнем 3,0 г% и 8 — с уровнем от 4,0 до 5,0 г%.
Экономическая эффективность бескровной хирургии
Средняя стоимость операции
| ||
Полное замещение тазобедренного сустава
|
Полное замещение коленного сустава
| |
Больные, участвовавшие в программе бескровного лечения
|
18 994 $
|
18 838 $
|
Больные, не участвовавшие в программе, но которым не переливали препараты крови
|
19 206 $
|
19 187 $
|
Больные, не участвовавшие в программе, которым переливали препараты крови
|
21 293 $
|
26 630 $
|
Нас часто спрашивают: «Разве лечение без переливания крови не стоит дороже?» Как видно из таблицы (несмотря на то, что разница относительно невелика), стоимость этих крупных ортопедических операций без переливания крови ничуть не выше таковых с переливанием. Бескровная хирургия снижает затраты на послеоперационное лечение и реабилитацию больных.
ВЫВОДЫ
(×) У системы гемоглобина огромные резервы
(×) Насыщение тканей кислородом зависит от множества факторов, а не только от уровня гемоглобина
(×) Уровень гемоглобина не всегда отражает состояние пациента и не должен служить основанием для переливания крови
(×) Вопрос достоинств и недостатков препаратов крови продолжает обсуждаться
(×) Существуют альтернативы переливанию донорской крови.
23. СНОСКИ
1. Доклад воспроизведён с аудиозаписи выступления на конференции «Острая кровопотеря» (г. Иваново, 21.10.99). Сохранён стиль устной речи, за исключением некоторых повторов (прим. ред.).




.bmp)
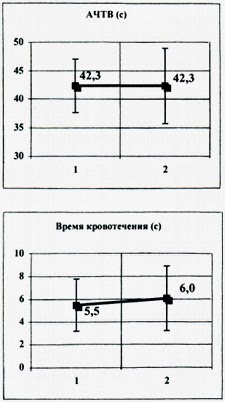

Комментариев нет:
Отправить комментарий